第一三共HER3 ADC第二项临床试验申请在中国提交
4月20日,CDE官网显示,第一三共HER3 ADC新药U3-1402提交新的临床试验申请。该药最早于2021年5月在中国申报临床,2021年11月启动临床试验。II期临床,针对EGFR突变NSCLC。
U3-1402项目详情
来自:Insight数据库小程序(http://db.dxy.cn/v5/home/)
HER3是HER酪氨酸激酶家族的成员之一表达在各种癌症中,可见于结直肠癌、胃癌、头颈鳞状癌、乳腺癌、肺癌等。HER3过表达与NSCLC癌细胞的转移与患者存活率的降低有关,因此有望成为晚期和转移性NSCLC新的治疗方法。
U3-1402是第一三共(DaiichiSankyo)一种抗体偶联药物正在研究中。抗体部分为HER3单抗patritumab(U3-1287),通过linker共价偶联拓扑异构酶I抑制剂依喜替康(exatecan,MAAA-1181a),每个抗体都有8个依喜替康。通过与癌细胞表面的表面相连。HER3结合,U3-1402依喜替康被吞入细胞释放,进而发挥细胞毒作用,杀死癌细胞。
抗体部分Patritumab是U3pharma与安进联合开发的靶向HER32008年第一三共收购单抗U3pharma,在研究中获得的patritumab及相关知识产权;2016年,由于临床数据不佳,第一三共终止Patritumab用于治疗NSCLC研发,但是ADC技术的出现使这种单抗焕发出新的活力,第一和第三共将其发展成为ADC药物,得到了U3-1402。
目前,U3-1402在国外进展到两期临床实践中,各大医学会议了8条数据。2021年,ASCO会议上,第一期和第三期更新了一期临床试验(NCT03260491)最新数据。
U3-1402项目详情
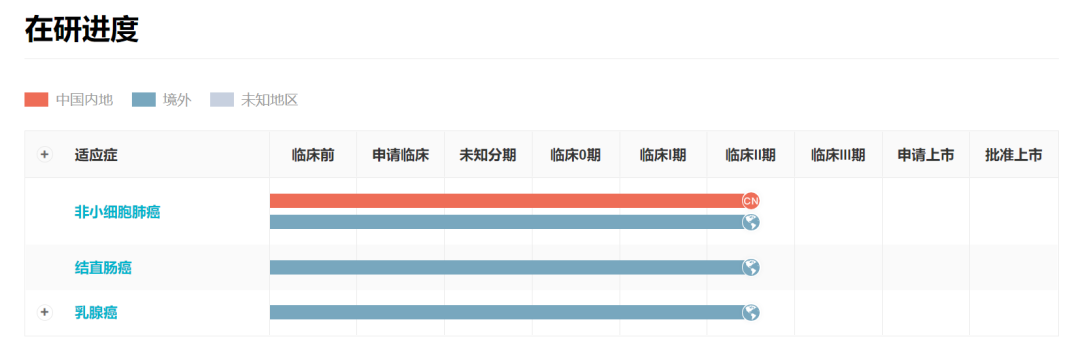
来自:Insight全球新药模块数据库(http://db.dxy.cn/v5/home/)
截至2020年9月24日,本次一期临床试验共入组57例NSCLC病人。这些病人以前都接受过。EGFR-TKI治疗,86%奥希替尼,91%含铂化疗,40%免疫治疗,中位治疗线数为4。其中包括27例脑转移。
结果显示,BICR客观缓解率的评价(ORR)39%的疾病控制率(DCR)72%,中位缓解持续时间(mDoR)为6.9个月,中位无进展生存期(mPFS)为8.2一个月。值得注意的是,44例之前接受过奥希替尼和含铂化疗的患者(图中)OSI疗效数据与其他患者相似。
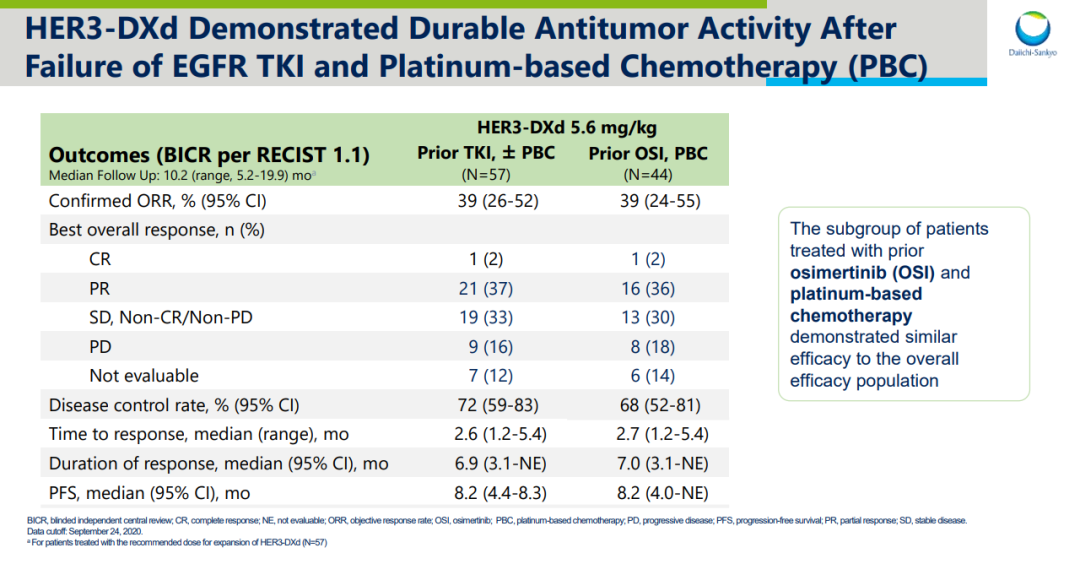
来自:2021 ASCO
在不同的机制中EGFR-TKI耐药患者中,U3-1402观察到肿瘤的部分缓解,包括肿瘤的缓解,EGFR C797S突变、MET基因扩增、HER2突变、BRAF整合等。耐药机制为耐药机制。EGFR患者,ORR达到47%;非EGFR/MET通路(包括KRAS、BRAF、ALK等)耐药患者,ORR达到45%。U3-1402它还显示了脑转移患者的活动,在脑转移患者中ORR为32%,DCR为80%,mPFS为8.2一个月,与无脑转移患者疗效相似。
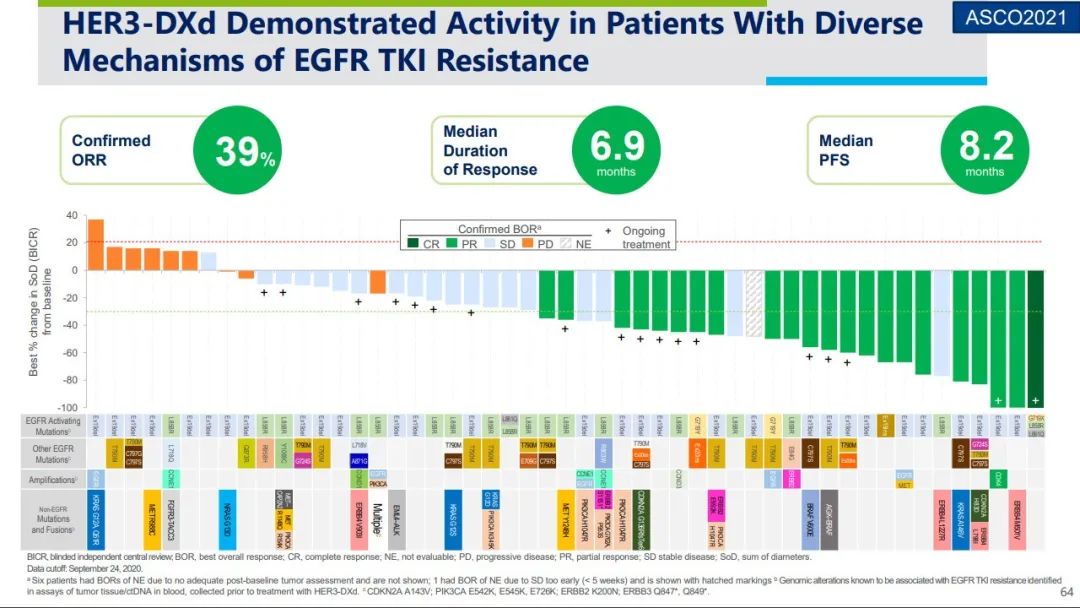
来自:2021 ASCO
值得注意的是,第一三共指出,HER3表达稳定,不受TKI治疗线数和时间的影响,因此,U3-1402对不同的耐药机制有疗效,可能会使更广泛的患者受益。而且,无论如何,无论是否。HER3表达高低,都有缓解病例。
基于一期临床临床的积极数据,第一阶段和第三阶段已经启动了第二阶段临床的关键数据HERTHENA-Lung01预计2022年完成研究。NSCLC之外,U3-1402也用于发展结直肠癌(CRC)乳腺癌适应症详见下图:

来自:第一三共官网
目前国内布局HER3目标企业很少。除第一、三共外,国内企业很少。HER3项目较多的企业是百利药业,该公司还有一家EGFR/HER3双抗SI-B001和EGFR/HER3双特异性ADCBL-B01D1,前者是最高的II在开发阶段,我们刚刚开始与奥希替尼联用EGFR突变NSCLC的II/III期临床;后者还在I期间开发阶段。
注:原文已被删除
