TNBC治疗突破:mRNA疗法 PD-L1抑制剂 大大提高了免疫疗法的疗效
文章来源:医药魔方Pro
作者:曼话
三阴性乳腺癌(TNBC)占所有乳腺癌的12%-20%,因雌激素受体(ER)、孕激素受体(PR)受体和人表皮生长因子2(HER2)它们都以阴性表达命名;与其他类型的乳腺癌相比,在年轻女性中更为常见;死亡率高,易复发转移;对激素治疗和靶向治疗不敏感,几乎只有化疗,但大多数患者很快就会产生耐药性,预后差;如果扩散到身体的其他部位,生存期通常只有一年左右。
以PD-1/PD-L1以抗体为代表的免疫检查点抑制剂能释放身体的抗肿瘤免疫反应,进而起到抗癌作用。尽管已经有了。PD-1/PD-L1三阴性乳腺癌(如帕博利珠单抗)被批准用于治疗(TNBC),但许多患者对这种免疫疗法没有反应或耐药性。最近,来自西班牙的一位科学家发现了一种有前途的方法,可以提高免疫检查点抑制剂治疗这种侵袭性乳腺癌的疗效。相关研究成果于3月17日发表Nature Cancer杂志上。
来自Hospital del Mar Medical Research Institute研究小组发现,在三阴性乳腺癌中,(TNBC)在中间,癌症干细胞可以避免免疫系统,一种叫做LCOR(ligand-dependent corepressor)蛋白质表达水平的增加会干扰这种免疫逃逸,使免疫系统看得见癌症干细胞,进而产生抗肿瘤作用。mRNA研究人员设计了一种疫苗启了一种疫苗mRNA疗法来生产LCOR。在小鼠中,这种mRNA疗法与抗PD-L1当检查点抑制剂联合使用时,抗肿瘤效果显著提高。
三阴性乳腺癌(TNBC)肿瘤干细胞可能占肿瘤总数的5%-50%,并可引起新肿瘤。LCOR介导乳腺癌干细胞的分化,所以研究小组想知道蛋白质是否在TNBC对检查点抑制剂的耐药性起作用。
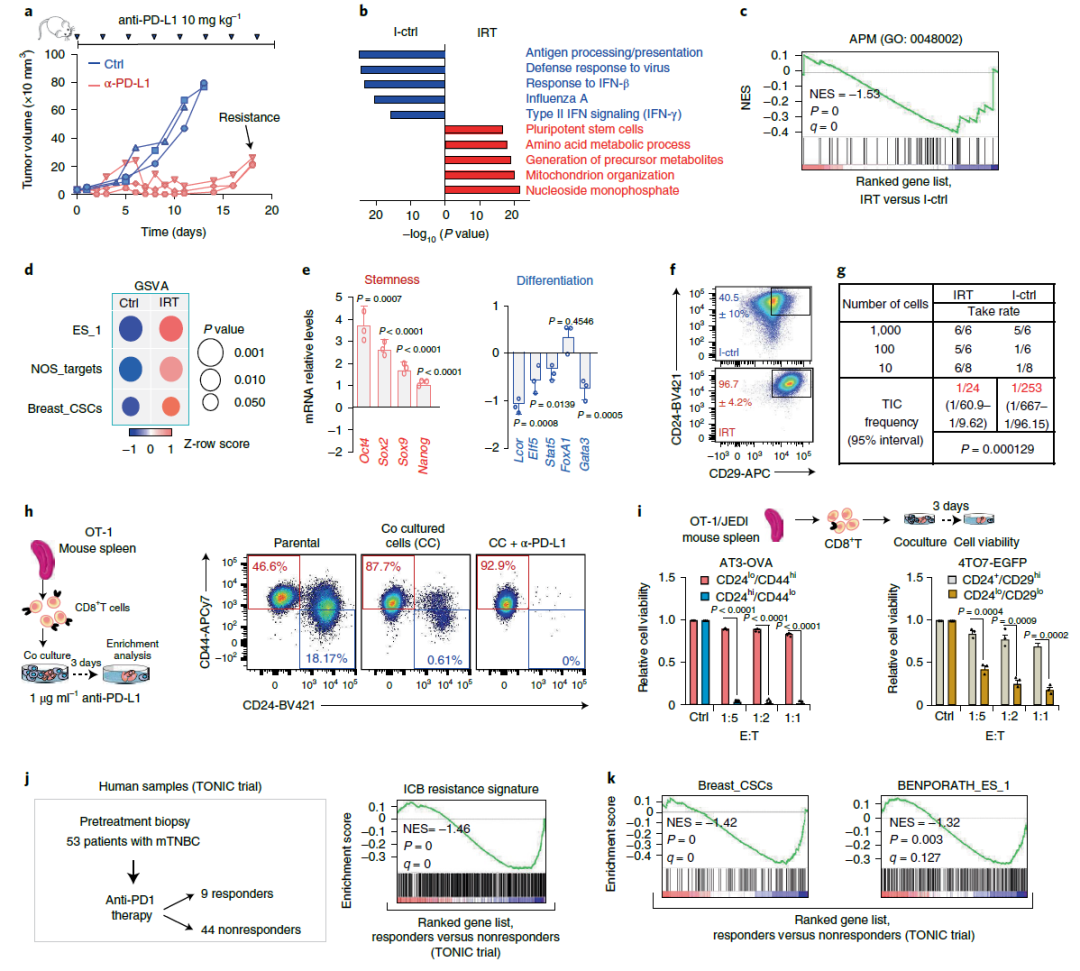
癌症干细胞(CSC)导致免疫编辑逃逸,免疫检查点抑制剂(ICB)耐药(来源:耐药:Nature Cancer)
来自小鼠的PD-L1科学家们发现,免疫治疗耐药肿瘤的研究,LCOR低表达水平的癌症干细胞抗原加工和呈现机制减少。向癌细胞表面提供抗原是免疫系统区分正常细胞和肿瘤细胞并攻击肿瘤细胞的关键步骤。
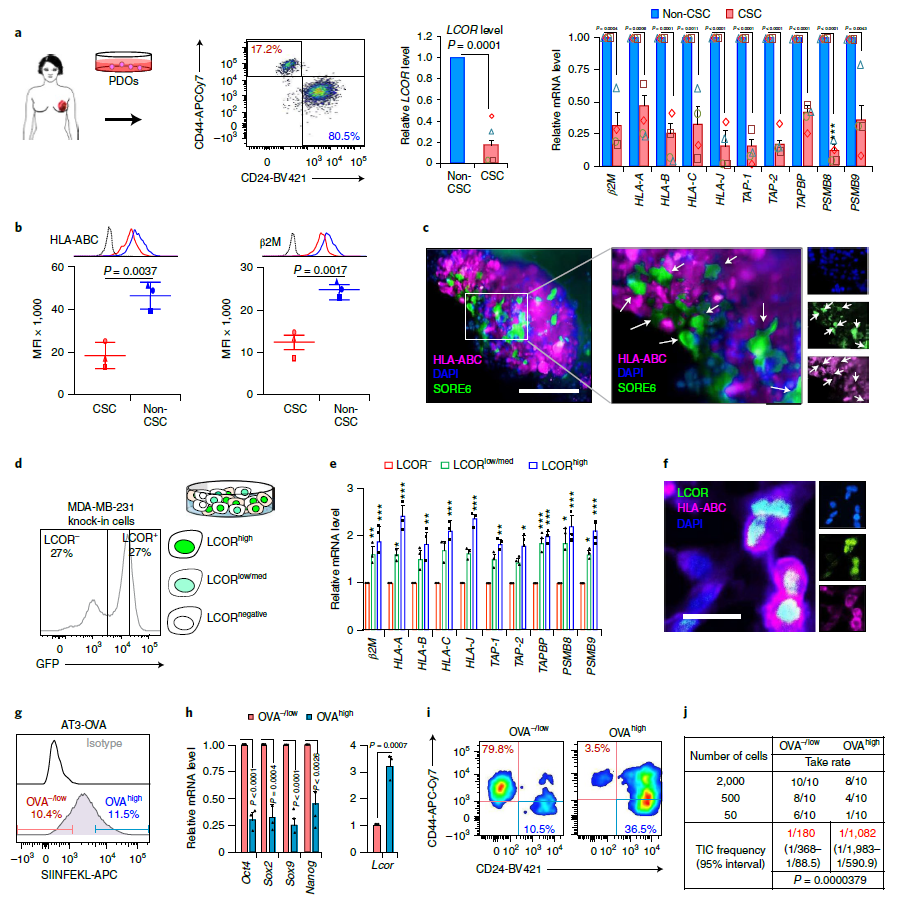
LCOR乳腺癌表达水平低CSC抗原呈递机制活性低(来源:Nature Cancer)
随后,研究发现,在实验室研究中,LCOR过表达的TNBC肿瘤细胞增多T细胞的激活表现为更多T细胞进入肿瘤并发挥杀伤作用。
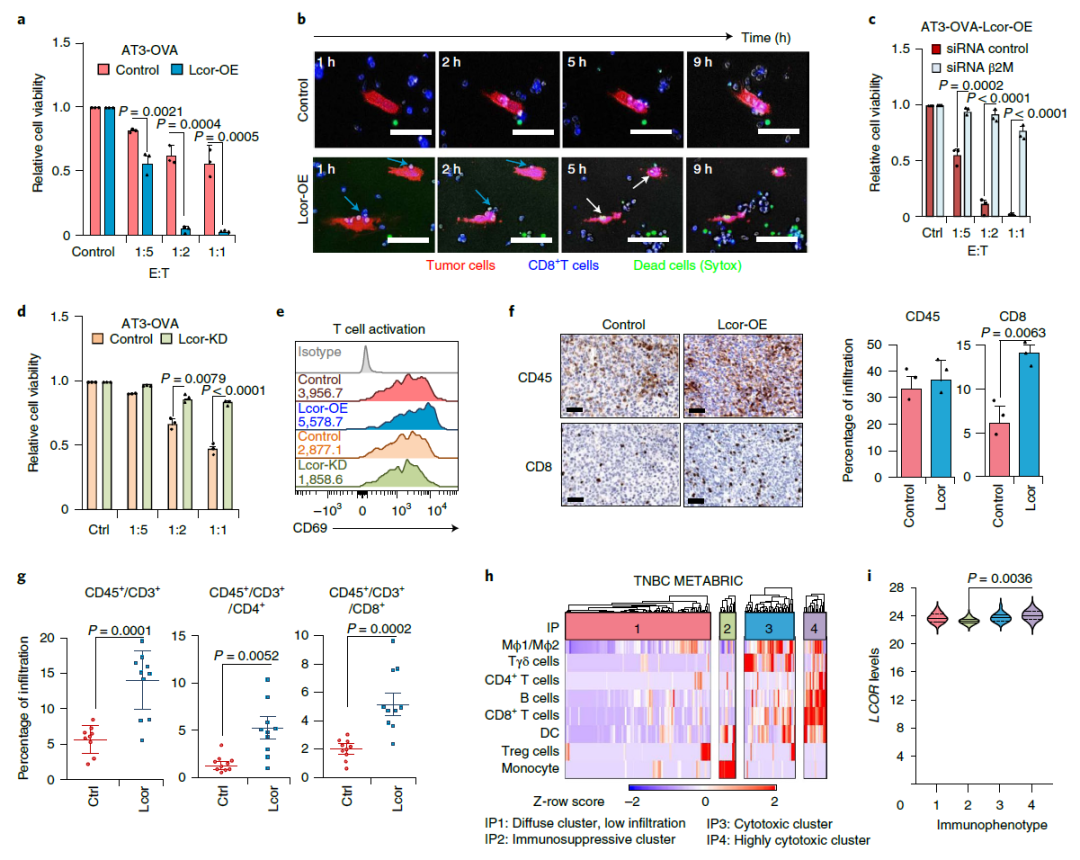
LCOR促进肿瘤免疫浸润和杀伤:Nature Cancer)
此外,科学家们还研究了一些来自TNBC这些患者参与了不同的肿瘤样本PD-1/L1抑制剂(包括Tecentriq、Opdivo和Imfinzi)临床试验LCOR表达与患者对这类检查点抑制剂的更好反应有关。
为了验证这一发现,科学家们在三阴性乳腺癌(TNBC)抗应用于小鼠模型PD-L1治疗方法。结果表明,与继续生长的对照肿瘤相比,接受抗PD-L1治疗,过表达LCOR肿瘤完全消退,所有小鼠在20天内不再有癌症迹象,达到完全缓解。
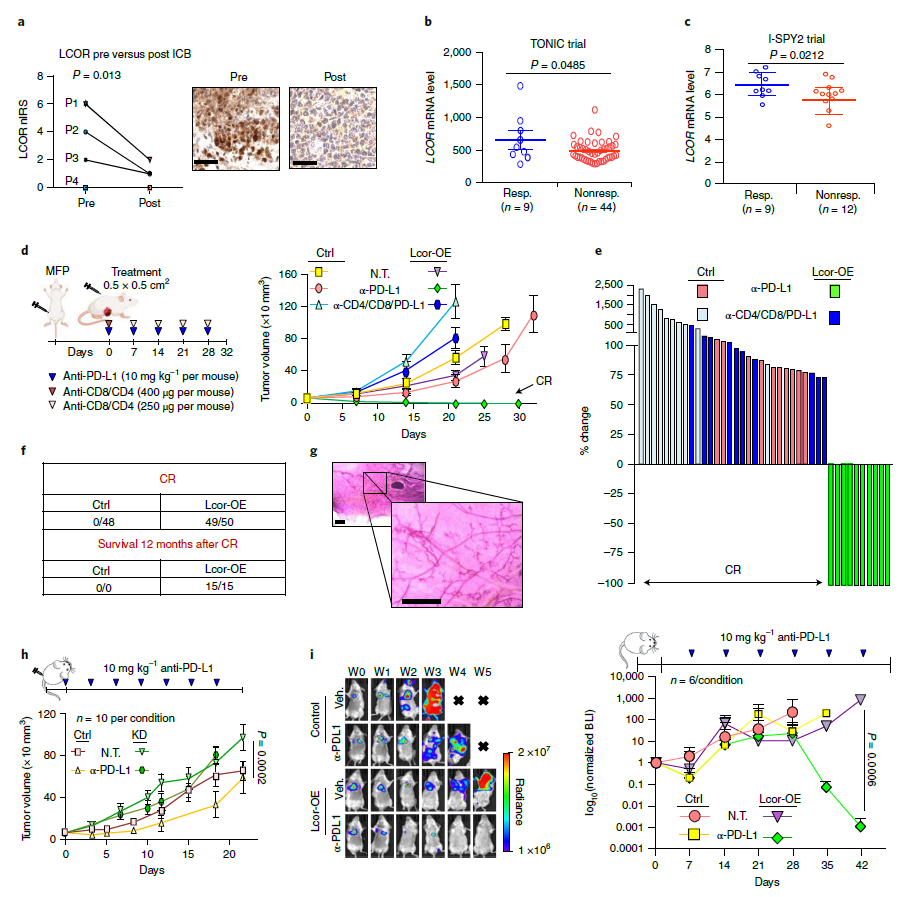
LCOR联合ICB临床前和临床意义(来源:Nature Cancer)
在5个独立实验中,研究小组观察到50个LCOR49个表达肿瘤完全缓解(CR)。值得注意的是,唯一未能完全缓解的肿瘤以某种方式缓解LCOR表达式丢失PD-L1治疗停止2个月后,全部49个达到CR乳腺保持无肿瘤状态。研究人员对其中15只小鼠进行了长达一年的随访,没有小鼠肿瘤复发,所有小鼠腺体都没有肿瘤(上图)f,g)。研究人员在论文中写道:这根除了肿瘤,治愈了这些小鼠。研究人员在论文中写道。
受新冠mRNA研究小组认为,通过传递疫苗的启示,通过传递mRNA表达治疗蛋白是一种可行的策略,所以他们设计了一种治疗蛋白mRNA恢复肿瘤细胞中的疗法LCOR表达。
在小鼠中,和PD-L1与单独治疗或对照治疗的抑制剂相比,LCOR mRNA联合治疗(通过细胞外囊泡)PD-L1抑制剂克服了肿瘤的耐药性,导致小鼠生存期显著延长,肺转移完全清除。
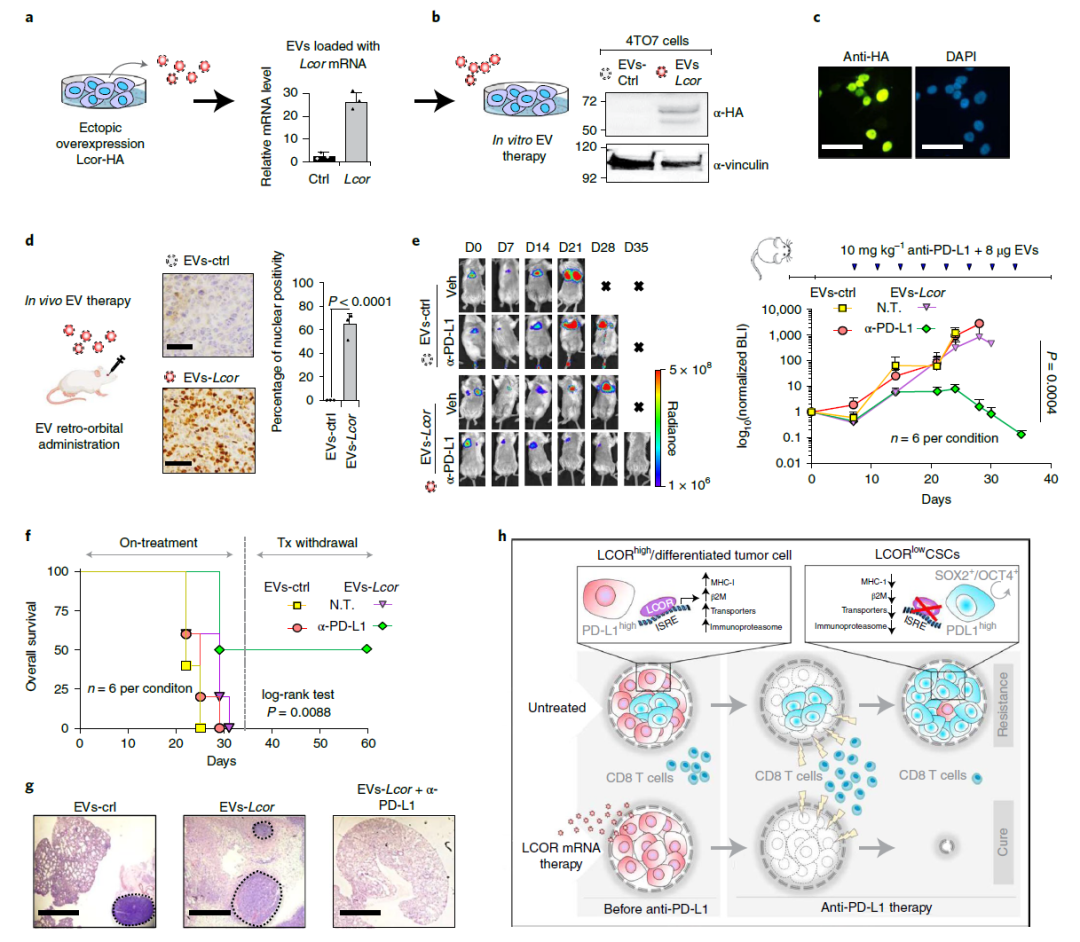
EV递送Lcor mRNA疗法联合ICB治疗乳腺癌转移的疗效
综上所述,科学家们认为这些数据支持LCOR作为改善检查点抑制剂治疗TNBC有效性是一个有希望的靶点。增加肿瘤细胞的抗原呈现,LCOR mRNA疗法可与PD-1/PD-L1抑制剂的联合使用有望大大改善免疫治疗TNBC的成功率。
注:原文已被删除

