5款上市 100款PSMA药物在研究 诺华,安进...
作者:笃行
近日,FDA批准诺华的177Lu-PSMA-617上市申请,用于治疗PSMA治疗进展后阳性、去势抵抗切列腺癌,商品名称为Pluvicto。近年来,一批企业加入其中PSMA药物研发,但部分药物临床进展不顺利,研发仍如履薄冰。177Lu-PSMA-617作为靶向PSMA辐射配体疗法的成功上市有望提振该目标的研发信心。
复合年增长率达到17.7%
靶向PSMA抗癌药物的出现
前列腺癌开始改变前列腺中的健康细胞,失去控制,最终发展成肿瘤,可能导致前列腺癌的风险因素包括BRCA1和BRCA2基因突变、其他遗传变化(HPC1、HPC2、HPCX、CAPB)、家族史和饮食习惯。
去势抵抗前列腺癌(CRPC)它是一种临床、放射学或生物化学恶化的前列腺癌。对于前列腺癌患者,在局部治疗后复发或扩散到远处的前列腺癌患者通常会阻断雄激素(ADT)然而,有反应,在接受中,ADT治疗后,大多数患者的病情会恶化并接受ADT18-24个月后发展成为CRPC,绝大多数CRPC会发展成为mCRPC。
据弗若斯特沙利文统计,中国CRPC2014年患者总数为2014年2.99万人按32.6复合年增长率的%增加到2018年9.25从2018年起,从2018年起按1万人,17.72023年复合增长率增长%20.9从2023年起,1万人,按压12.62029年复合年增长率增长%37.76万人。
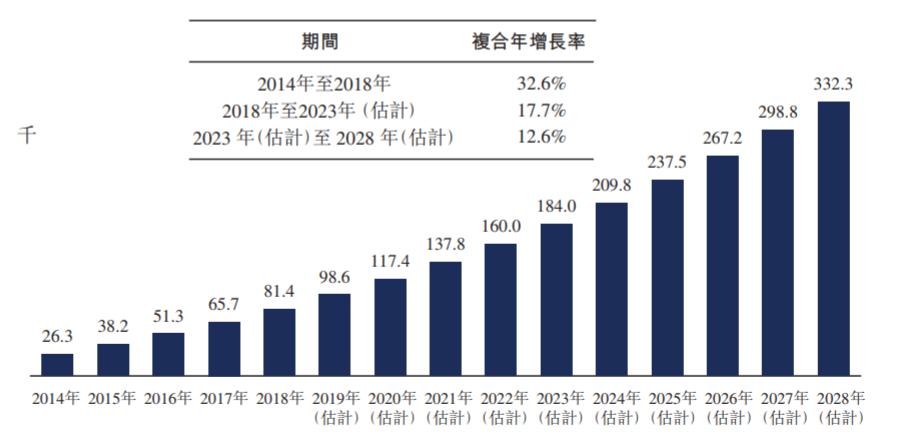
图:2014-2028年中国mCRPC患者总数
数据来源:弗若斯特沙利文
目前,mCRPC多西他赛、恩扎卢胺和阿比特龙主要用于一线治疗。然而,无论是阿比特龙还是恩扎卢胺,在服药一段时间后耐药性,通常是18-20一个月。对于耐药患者,二线治疗尤为关键,目前化疗是化疗的关键。mCRPC二线治疗的首选,此外,靶向治疗PSMA抗癌药物如雨后春笋般涌现,包括ADC、双抗、CAR-T等待新疗法。
PSMA 靶点介绍和创新疗法
100研究型,5款已上市
前列腺特异性膜抗原(PSMA,Prostate Specific Membrane Antigen)它是前列腺细胞的特异性肿瘤标志物。研究发现,PSMA在正常的前列腺组织中低表达,但在大多数前列腺癌组织中高表达;此外,在前列腺癌的进展中CRPC在这个过程中,许多前列腺癌细胞可能会失去前列腺特异性抗原(PSA),但PSMA还能保留,所以PSMA这是一个潜在的前列腺癌靶标。PSMA前列腺癌的生物学功能尚未得到充分的研究,研究表明它可以释放谷氨酸作为信使分子激活细胞的信使PI3K-Akt参与前列腺癌细胞增殖、迁移和生存的信号通路。
据不完全统计,目前,针对不完全统计,PSMA研究药物近100种,其中5种获批上市。但其中四种都是。PSMA靶向PET成像药用于指示体内存在的成像药物PSMA阳性前列腺癌病变。诺华的。177Lu-PSMA-617是第一个将靶向的PSMA结合治疗性放射性同位素的精确癌症治疗可显著降低患者的死亡风险。其他靶向癌症治疗方法。PSMA创新疗法包括放射性配体疗法(RLT)、ADC、双抗、CAR-T等。
(1)RLT/RDC药物:诺华的177Lu-PSMA-617是一种靶向PSMA通过放射配体疗法,PSMA小分子靶向药物PSMA-617与放射性同位素177偶联。177Lu-PSMA-617通过PSMA分子定位前列腺癌细胞群,在不影响周围细胞的情况下,将放射源传递给前列腺癌细胞进行精确辐射。
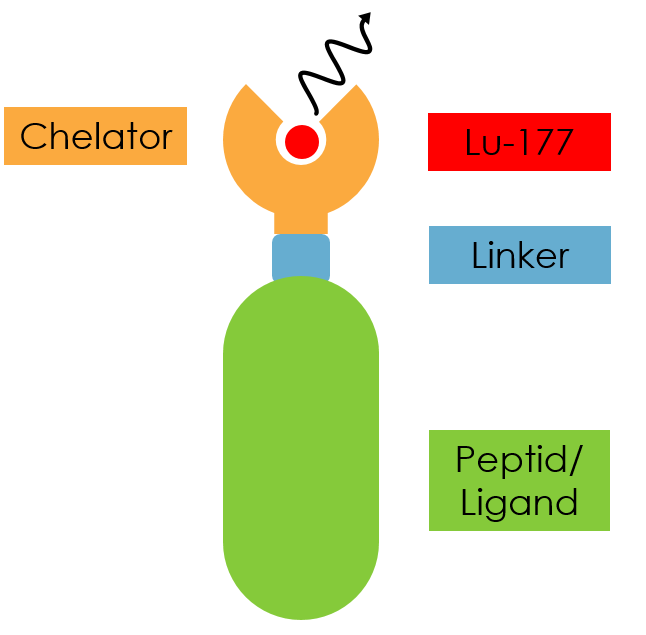
图:177Lu-PSMA-617结构
数据来源:诺华
2021年ASCO,诺华公布了177Lu-PSMA-617的Ⅲ临床研究数据。2018年7月至2019年10月,831名接受雄激素受体抑制剂和紫杉烷化疗的患者以2:1的比例纳入177Lu-PSMA-617 SOC组(n=551)和SOC组(n=280)。结果显示,试验组PFS和OS显著改进,试验组和对照组PFS为8.7 vs 3.4m,OS为15.3 vs11.3m,ORR为29.8% vs 1.7%,DCR为89% vs66.7%。不良事件方面,试验组不良事件发生率略高于对照组,严重不良事件风险率为52.7% vs38.0%。来说,从OS的角度,177Lu-PSMA-617数据不是特别亮眼,但考虑到数据不是特别亮眼,mCRPC目前缺乏更好的治疗方法,177Lu-PSMA-617填补了mCRPC晚期治疗的空白。
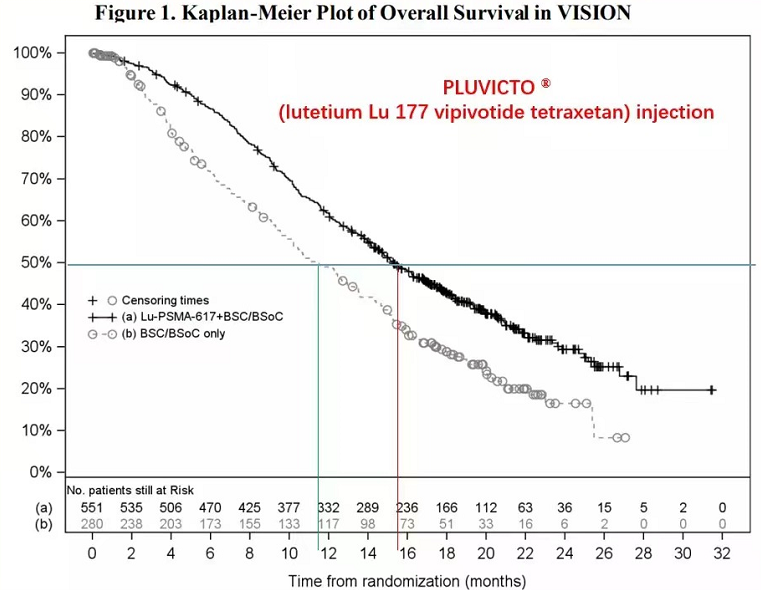
图:177Lu-PSMA-617 Ⅲ期OS数据
数据来源:诺华
(2)ADC药物:ARX517是Ambrx研发的目标PSMA抗体偶联药物,由全人源抗体PSMA单抗和两种微管蛋白抑制剂AS269构成。AS269全称Amberstatin269,为Ambrx专有、强效的微管蛋白抑制剂能与抗体中的合成氨基酸形成高度稳定的共价键。临床试验中,ARX517在恩扎卢胺敏感性和耐药性前列腺癌模型中表现出活性。2021年8月,Ambrx宣布ARX517完成Ⅰ第一例临床病例给药。
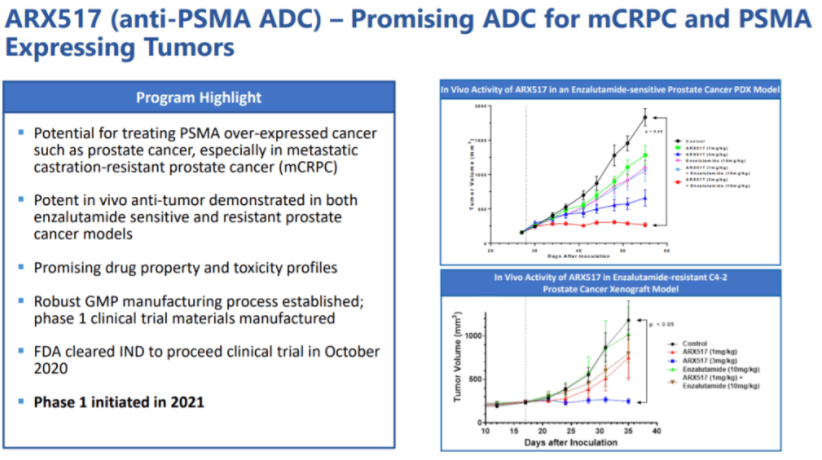
图:ARX517产品亮点
数据来源:Ambrx
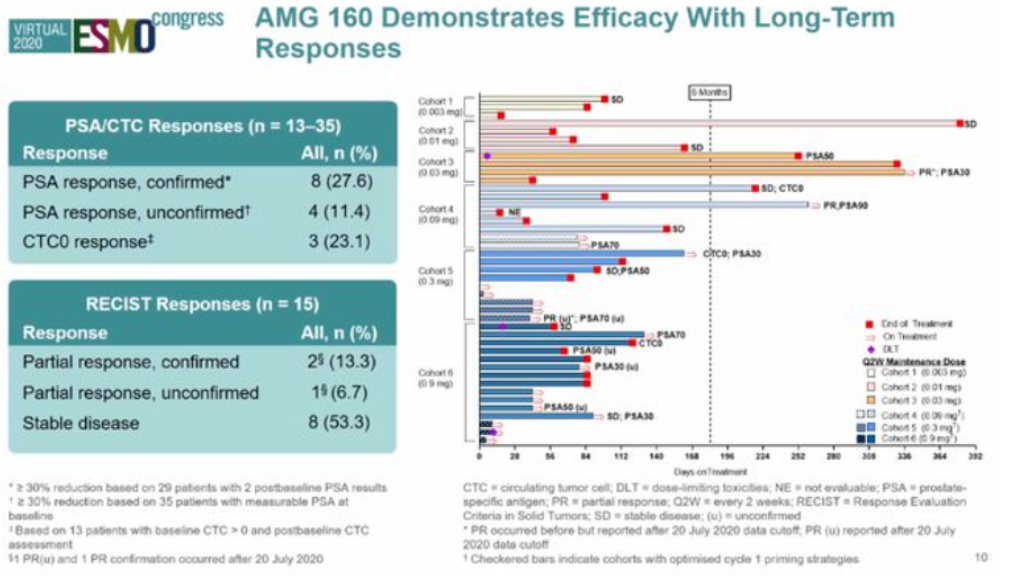
(3)双抗药物:AMG160(acapatamab)是安进/百济神州开发的一款CD3×PSMA双抗,用于治疗成人转移性去势抵抗前列腺癌,目前处于临床实践中Ⅰ期。AMG160通过与肿瘤细胞的 PSMA 和 T 细胞上的 CD3 结合,使 T 细胞定向杀伤PSMA肿瘤细胞的高表达。AMG160基于安进的HLE-BiTE平台研发,和BiTE不同,HLE-BiTE引入平台Fc该地区延长了药物的半衰期。
在2020 ESMO上,安进公布AMG160的Ⅰ期临床数据,确认PSA缓解率达27.6%,SD达53.3%,证实了AMG160对mCRPC具有初步疗效AMG16020%患者的免疫原性存在一定问题ADA影响药物暴露水平的水平。2021年7月,安进收购了Teneobio,Teneobio旗下的TNB-585亦是一款CD3×PSMA双抗,通过强强联合,安进有望在CD3×PSMA双打赛道更进一步。
HPN424是由Harpoon Therapeutics一种基于三特异性抗体的三特异性抗体。TriTac平台研发。HPN424除了靶向T细胞表面CD3肿瘤细胞表面PSMA此外,还含有一段人血清白蛋白,以改善抗体半衰期。因为不含。Fc区域,TriTac其分子量仅为单抗的1/3,对实体瘤具有较强的穿透能力。2021年3月,Harpoon Therapeutics宣布放弃HPN424研发的原因是潜在的ADA受此消息影响,公司股价下跌27%。事实上,根据公司在公司的情况,2021ASCO公布的HPN424Ⅰ期数据,缓解率有限(PR=6.67%)和较高的安全风险在一定程度上预示着研发失败。
图:HPN424示意图
数据来源:Harpoon Therapeutics
(4)CAR-T疗法:P-PSMA-101是Poseida公司研发的目标PSMA 的自体CAR-T疗法。该疗法已被使用Poseida专属非病毒piggyBac DNA修饰系统开发,系统生产的候选产品具有高比例的干细胞样记忆T细胞(TSCM)。与其他CAR-T细胞相比,TSCM细胞具有自我更新能力,产品疗效有望更持久,毒性更小。
2020年5月,P-PSMA-101启动了治疗mCRPC的Ⅰ期临床研究。今年7月,一名受试者死于肝功能衰竭,因此,受试者死于肝功能衰竭。FDA叫停。Poseida该公司解释说,该症状是巨噬细胞活化综合征(MAS),它是由免疫系统的过度激活引起的。11月,在11月,在11月。Poseida在改变试验方案以提高患者的依从性和药物安全性后,FDA解除了对试验的临床限制。
2022年2月,在2022 ASCO GU上,Poseida公布了P-PSMA-101的Ⅰ在14名可评估、平均接受过七线治疗的患者中,71%的患者出现了期中期结果,PSA水平明显下降,36%的患者PSA水平下降>50%,1名患者肿瘤完全消除,持续缓解10个月以上。安全方面,2名患者有3级以上。CRS(14.2%),包括以前的出现MAS病人。一般来说,中期数据结果令人鼓舞,P-PSMA-101疗效和安全性都很好。
小结
目前,靶向PSMA创新疗法包括放射性配体疗法(RLT)、ADC、双抗、CAR-T等等。其中,诺华177Lu-PSMA-617是第一个将靶向的PSMA结合治疗性放射性同位素的精确癌症疗法于3月22日获得FDA批准上市PSMA双抗疗法进展不顺利,ADA是主要问题。CAR-T疗法经历被FDA停牌后,目前披露Ⅰ中期数据令人鼓舞。ADC药物由全球ADC龙头企业Ambrx操刀,目前处于Ⅰ早期。衷心祝愿靶向靶向。PSMA创新疗法进展顺利,晚期创新疗法进展顺利mCRPC患者提供新的治疗方法。
