传奇生物cilta-cel成功出海 盘点CAR-T竞争格局!
作者:骆南
2022年2月28日,本应于去年11月底结束的审查推迟三个月后,FDA最于批准了由中国制药公司传奇生物自主研发的靶向B细胞成熟抗原(B cell maturation antigen,BCMA),成人复发/难治性多发性骨髓瘤(R/RMM)治疗的CAR-T产品cilta-cel。
传奇生物的cilta-cel它有两个靶向BCMA单域抗体的CAR-T细胞免疫疗法,以一次性输液的方式给药。本次审批以关键研究为基础。CARTITUDE-1 Ib/II积极数据。
CARTITUDE-1结果显示,97例R/R MM患者有早期、深度、持久的缓解,总缓解率(ORR)高达98%(95%CI:92.7-99.7),78%的患者得到了严格、完全的缓解(sCR,95%CI:68.8-86.1)。在18个月的中位随访时间中,中位缓解持续时间(DOR)为21.8个月(95% CI,21.8-不可预测)。
传奇生物cilta-cel全球第七款上市CAR-T产品,是美FDA批准的第六款。当其他的时候。CAR-T产品扎堆于CD19靶点时,cilta-cel选择竞争相对较小的选择BCMA靶点。
针对BCMA靶点的CAR-T以前只有一个,是的BMS和蓝鸟研发Abecma(ide-cel),于2021年3月获得FDA批准。
2017年12月,传奇生物与杨森签署了全球独家许可和合作协议,以开发和商业化cilta-cel。据悉,它在美国的定价是46.5万美元,根据Evaluate Vantage的估测,cilta-cel2026年销售额可达17亿美元。
根据弗若斯特沙利文的数据,全球数据,CAR-T2017年细胞治疗市场从2017年开始0.1亿美元增加到2019年的7亿美元和2020年的11亿美元,预计未来几年将加速增长,2024年将扩大到66亿美元,2030年市场将进一步增长到218亿美元。
借此机会,笔者在这里盘点一下目前其他六款CAR-T产品,一窥传奇生物的批准将如何搅动CAR-T产品竞争格局,引起什么样的波澜。
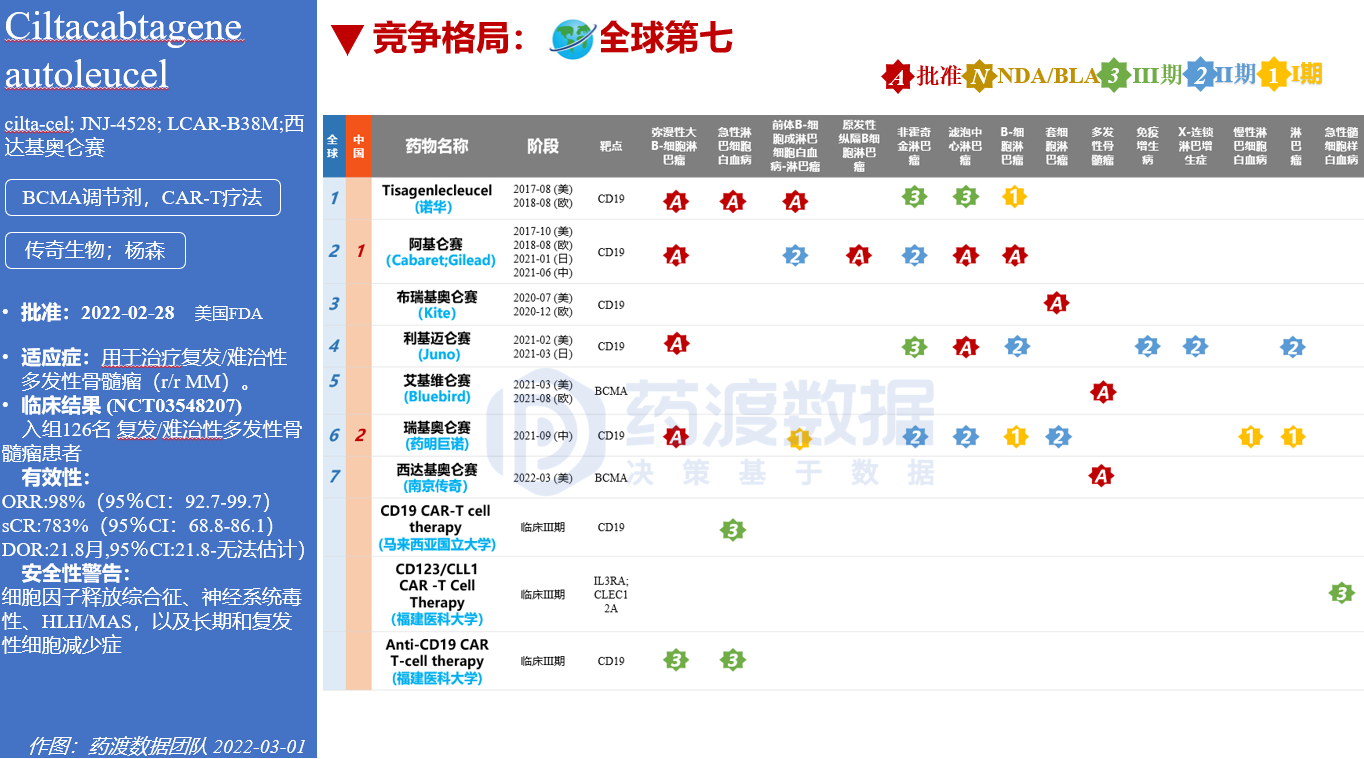
诺华:Kymriah?(tisageniducel)
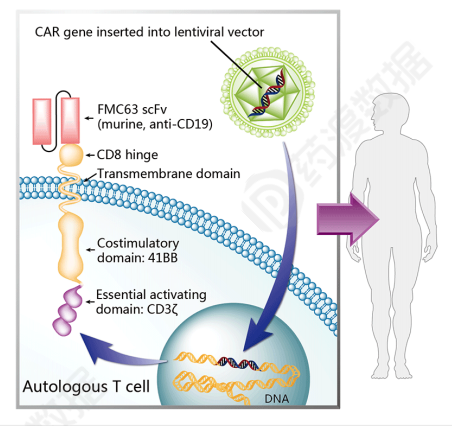
结构信息
相比tisagenIecIeucel,Kymriah?自2017年上市以来,该017年上市以来,一直占据主导地位CAR-T药物的半壁江山。
作为FDA第一个批准也是世界上第一个CAR-T细胞疗法,Kymriah?上市具有里程碑意义。
Kymriah?靶向CD19,治疗病人B急性淋巴性白血病(ALL),25岁以下患者病情难治或复发两次以上。2018年,新的适应症被批准用于治疗复发或难治性弥漫性B细胞淋巴瘤(DLBCL)成人患者(以前接受过两次以上的系统治疗),同年获得EMA的批准。
根据药渡数据库查询,Kymriah?目前,我国仍处于临床三期试验状态,适应症为非霍奇金淋巴瘤。具体研发阶段如下图所示。
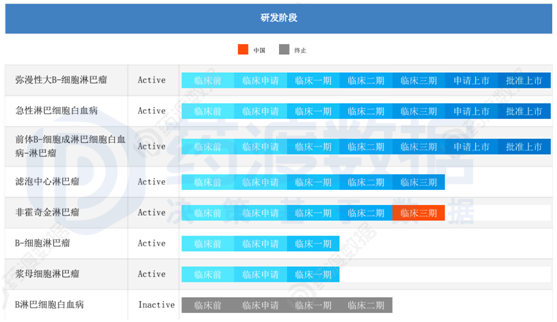
目前Kymriah?已在全球30个国家上市,有350多个认证治疗中心。
北京三水生物科技有限公司和上海西比曼生物科技有限公司是国内引进公司。2018年,诺华与西比曼生物达成战略合作协议,西比曼生物负责中国的生产和供应Kymriah?,诺华将成为营销许可证的独家持有人。
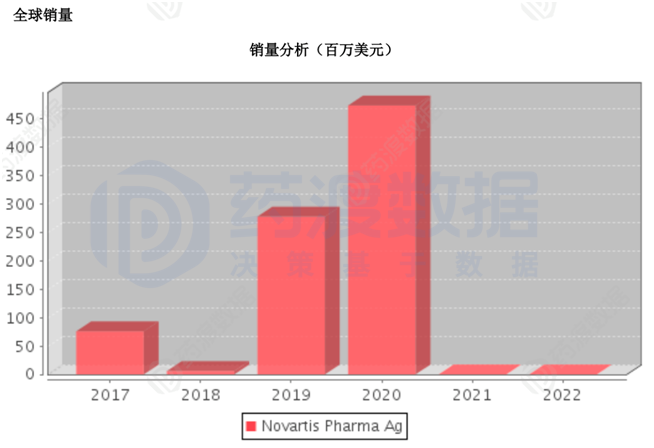
2020年,Kymriah?销售了4.74亿美元,同比增长68%。
Cabaret和吉利德:Axicabtagene ciloleucel(阿基仑赛)
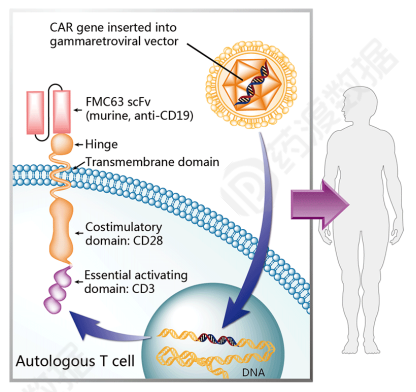
结构信息
201710月份,阿基仑赛获得美FDA批准用于治疗复发/难治性B成人细胞淋巴瘤患者。2018年,阿基仑赛和阿基仑赛与阿基仑赛。Kymriah?8月份一起获得EMA批准。
2017复星医药和吉利德科学控股子公司美国Kite Pharma复星凯特于4月在上海注册,成立了合资企业。复星凯特在中国大陆、香港和澳门获得了阿基仑赛的技术和商业权利。
20212006年6月22日,阿基仑赛获中国国家药品监督管理局称号NMPA批准已成为我国首次正式批准上市CAR-T细胞治疗产品,商品名称为易凯达。下图显示了各种适应症的进展。

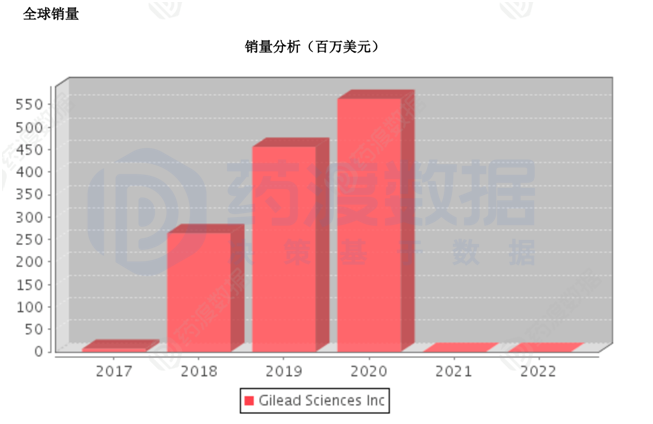
阿基018年开始,阿基仑赛的销售额逐年增长2.64到2019年,1亿美元的销大幅增长,达到4.56亿,2020年增长23%5.63亿美元。
Kite Pharma 和吉利德科学:Brexucabtagene autoleucel(布瑞基奥仑赛)
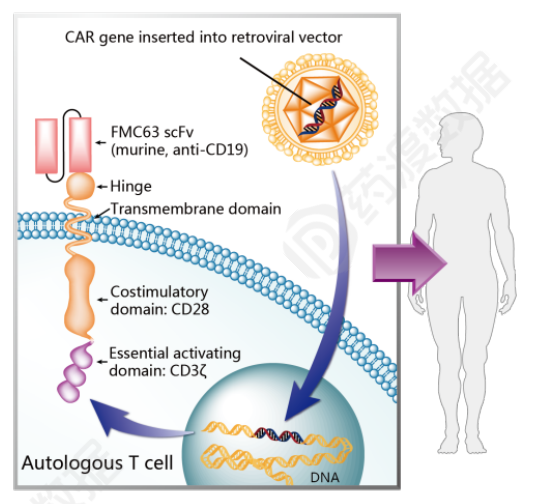
结构信息
布里基奥仑赛是第三个目标CD19的CAR-T该产品也是第一款用于治疗套细胞淋巴瘤的产品CAR-T产品。
2020布瑞基奥仑赛于7月获得FDA同年12月获得批准,同年12月获得批准EMA批准用于治疗复发或难治性套细胞淋巴瘤成人患者,定价为37.3万美元。目前在中国尚未申报上市。

目前,美国正在进行多项临床试验,进展最快的是套细胞淋巴瘤和血液肿瘤,正处于临床二期阶段。
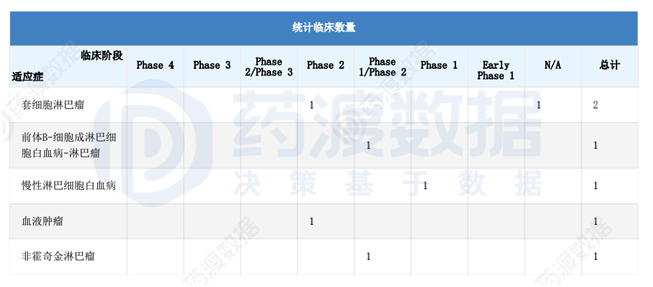
2020布瑞基奥仑赛年销售额达到4400万美元。
Celgene/Juno Therapeutics:Lisocabtagene maraleucel(利基迈仑赛)
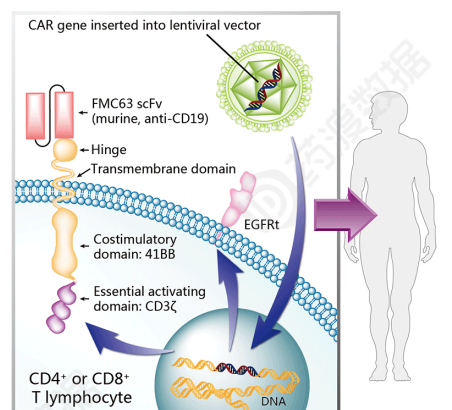
结构信息
利基迈仑赛是BMS(BMS收购了Celgene)一个目标CD19的CAR-T该产品用于治疗滤泡中心淋巴瘤和弥漫性大B-细胞淋巴瘤,由阿斯利康和阿斯利康和Memorial Sloan Kettering Cancer Center研发。
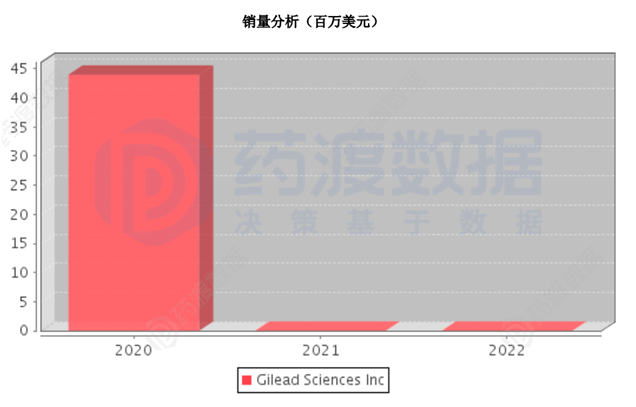
20212月5日,利基迈仑赛获美FDA批准,届时由BMS销售,定价为42.03万美元。同年3月25日,日本获得2021年3月25日,利基迈仑赛获得日本医药和医疗器械局PMDA批准,由Celgene Corp销售。但目前还没有在中国申报。
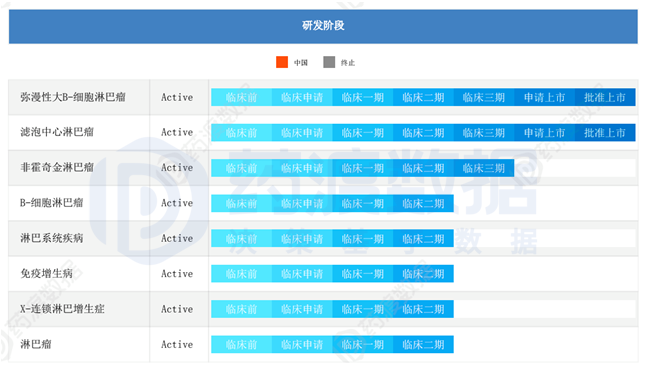
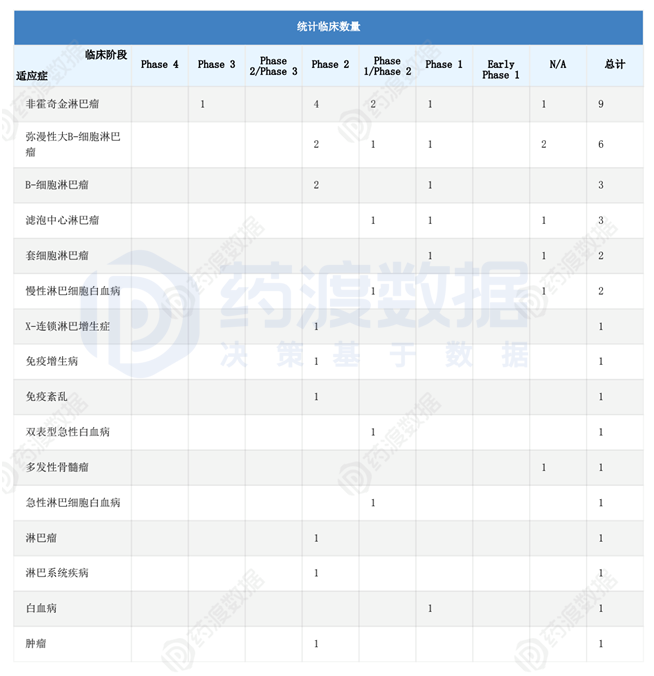
与此同时,利基迈仑赛正在美国进行多次临床试验。
Bluebird Bio/BMS:Idecabtagene vicleucel(艾基维仑赛)
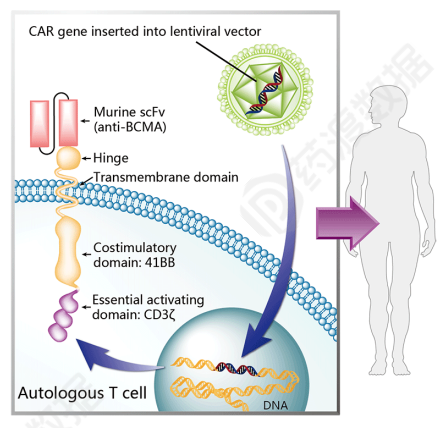
结构信息
艾基维仑赛是第一个针对艾基维仑赛BCMA靶点的CAR-T该产品用于治疗多发性骨髓,也被视为传奇生物cilta-cel强大的竞争对手之一。
2021年3月26日,艾基维仑赛获得美国FDA批准上市,由Celgene Corp销售。同年8月,得到的,得到的。EMA批准,由BMS销售,商品名称Abecma?。
Abecma?定价为41.95万美元,行业预计销售峰值为万美元,6.29亿美元。这一估计是基于此。Abercma?作为治疗 MM5线疗法,适应人群非常有限。这也是强生/传奇生物的。cilta-cel留下更大的空间,即通过更前线的适应症抢占BCMA靶点的CAR-T市场。

目前,艾基维仑赛正在美国进行多项多发性骨髓瘤临床试验。

药明巨诺:Relmacabtagene autoleucel(瑞基奥仑)
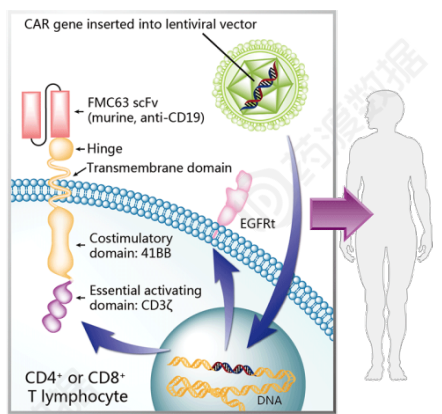
结构信息
2016年,药明康德和CAR-T制药公司Juno成立合资公司药明巨诺,共同开展CAR-T和TCR(T细胞抗原受体)疗法的研发与生产。2018年1月,新基以90亿美元的价格收购了新基。Juno。2019年1月,BMS投资740亿美元收购新基。
20212000年,药明巨诺发布公告称,其CAR-T瑞基奥伦赛注射液(商品名:倍诺达)已获得NMPA批准。这是继复星凯特阿基仑赛注射液(商品名称:易凯达)之后,国内第二款获批。CAR-T全球第六款获批上市的疗法和疗法CAR-T产品。
瑞基奥仑赛的目标CD19,治疗弥漫性大B-细胞淋巴瘤。
20221月,上海明聚生物科技有限公司在中国大陆开展了治疗前体的工作B-淋巴细胞白血病-淋巴瘤的临床试验和套细胞淋巴瘤的临床试验。同年12月,明聚生物在中国大陆进行了慢性淋巴细胞白血病和淋巴瘤的试验。
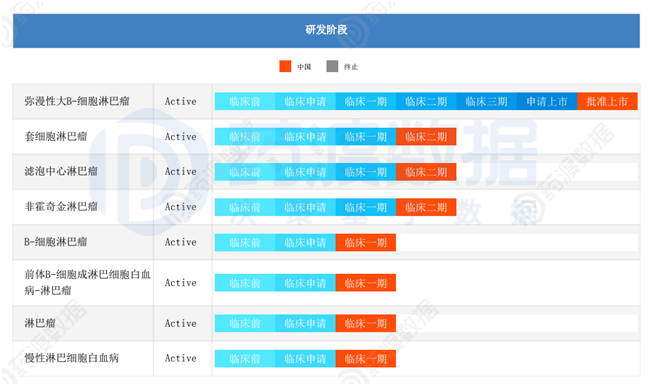
与此同时,药明巨诺也在美国推广多项临床试验。
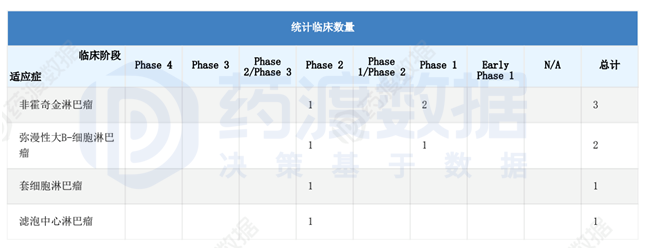
结语
Kymriah?与阿基仑赛有先发趋势,利基迈仑赛安全性极佳,只有一个布瑞基奥仑赛适应症套细胞淋巴瘤,面对同样的情况BCMA靶点的Abecma?国内第二款获批,国内第二款获批。CAR-T治疗瑞基奥仑赛,cilta-cel价格上没有优势。
但传奇生物CEO黄颖博士在cilta-cel在新闻发布会上,我不介意这一点。我认为定价在合理的范围内,并依靠它cilta-cel优秀的数据将给患者带来积极的临床效益。
当我们回顾国内市场时,企业很多CAR-T科济生物、西比曼生物、驯鹿医曼生物、驯鹿医疗、永喜生物等。
根据弗若斯特沙利文的数据,全球数据,CAR-T2020年细胞治疗市场将达到11亿美元,预计未来几年将加速增长,2024年将扩大至66亿美元,2030年市场将进一步增长至218亿美元。
这么大的市场,谁会统治,慢慢看……
数据来源:整理自药渡数据库
