72%的R&D管道来自他们!新兴制药公司的时代已经到来
新兴的生物医学公司是生物医学创新的重要引擎之一,其中许多公司正处于科学转型的前沿。随着时间的推移,他们开发的一些产品可以成功地上市。在其他情况下,这些产品或整个公司被更大的公司收购,以促进创新药物的出现。几天前,IQVIA人类数据科学研究所(IQVIA Institute for Human Data Science)发布了名为Emerging Biopharma’s Contribution to Innovation我们的研究报告介绍了新兴生物医学公司对创新的贡献。在今天的文章中,姚明康德内容团队将与读者分享报告的精彩内容,并点击文章末尾的阅读全文/Read more,即可浏览英文报告全文。
新兴生物医药公司临床期R&D管道增长89%
在这份报告中,新兴生物医药公司(EBP)定义为生物医药和生物技术公司,自2014年以来,处方药年销售额不足5亿美元,研发投资不足2亿美元。报告指出,2021年,这些公司参与了4500多种临床研究产品的开发,占目前临床研发管道的72%,EBP2021年,独立开发的产品占临床研发管道的65%,达到历史新高。
报告指出,总体而言,临床研发管道在过去10年中增长了85%,而89%的增长可以归结为EBP公司成长。这些数字显示了他们在开发创新疗法方面的贡献。
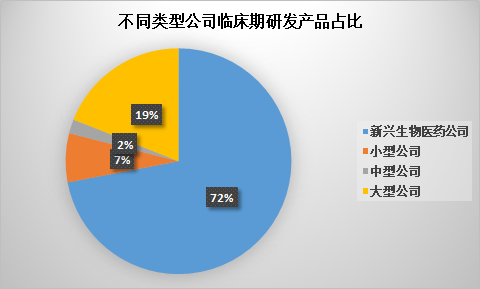
▲临床期研发管道在不同类型公司中所占比例(数据来源:参考资料[1],医明康德内容团队制图)
在过去的五年里,EBP公司开发的在研产品数量翻了一番,90%EBP公司的研发活动集中在美国、欧洲、中国、日本和韩国。
总部位于美国EBP公司开发的产品占比EBP近50%的研发管道,但占比近年来有所下降。总部设在中国EBP公司开发的产品是EBP近年来,R&D管道的比例迅速上升,自2006年以来增长了456%,2021年达到17%。这些数据也显示了中国新兴企业对药物研发和创新的贡献。
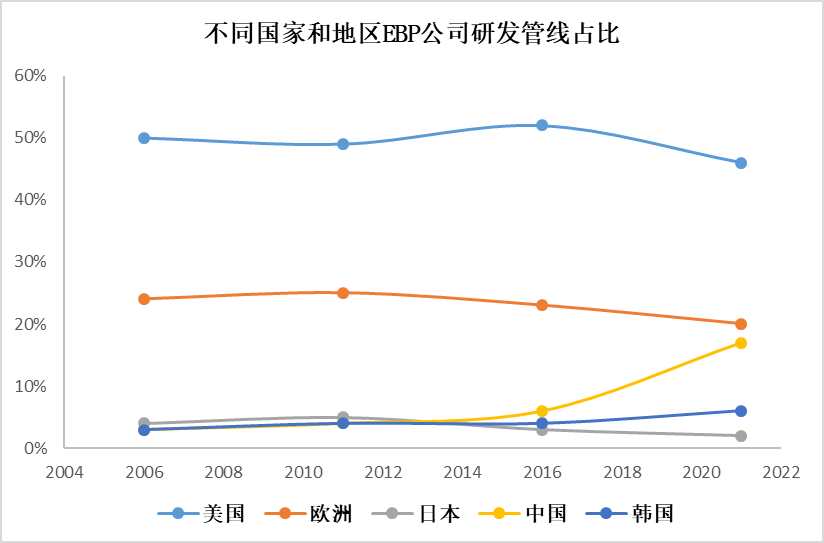
▲不同的国家和地区EBP公司临床期R&D管道占比(数据来源:参考资料[1],医药康德内容团队制图)
在美国,EBP在欧洲,该公司参与了近三分之二的研发活动,涉及开发多种产品,在欧洲,EBP公司参与47%的药品开发活动。在中国和韩国,EBP公司牵头开展药品研发活动,分别参与新药开发活动的76%和83%。这些数字也凸显了药物研发公司在这些国家的投资和成长。
肿瘤学、神经病学、传染病、胃肠道产品和疫苗在研发产品的适应症中占比EBP69%的研发管道。其中,肿瘤学管道的数量在过去五年中翻了一番,占了一半EBP39%的研发管道。在过去的两年中,传染病治疗和疫苗开发显著增加,这反映EBP公司对新冠疫情的贡献。
2021年递交FDA监管申请占比42%
在2021年,EBP与10年前相比,公司牵头启动了3386项临床试验,几乎翻了三倍。EBP公司主导的临床试验也是临床试验数量增加的主要原因。2021年,EBP临床试验导的临床试验占总数的59%,达到历史最高水平。
从2010年以来,EBP公司启动的研发项目整体临床开发成功率高于非非非临床开发项目EBP公司略高,尤其是在研发初期。
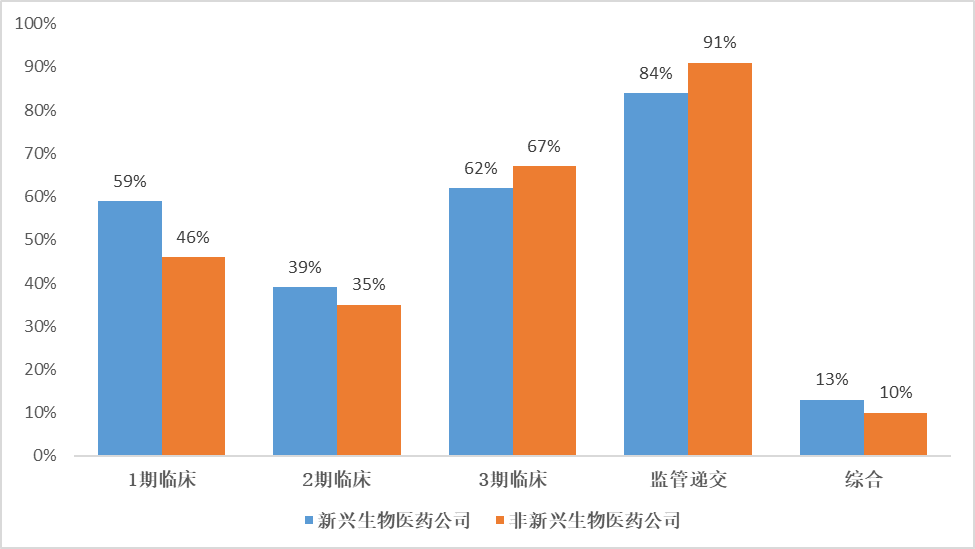
▲2010-2021年间,不同临床开发阶段的平均R&D成功率(数据来源:参考资料[1],医药康德内容团队制图)
在2021年,EBP公司向FDA与2012年(11%)相比,提交的产品上市监管申请占总数的42%增长了近4倍。这一趋势表明EBP公司有能力独立开发产品,直到上市。
研发产品“first-in-class”比例更高
报告指出,EBP公司正在推动包含创新活性物质的工作(novel active substances,NAS)药品上市也有重要贡献。2021年,全球上市NAS药85种药物,其中48种最初由EBP公司发展,达到历史最高水平。在美国,EBP最初由公司开发NAS药品占2021年上市药品的一半。EBP在公司最初开发并最终上市的药品中,由EBP公司自行提交FDA申请监管的药品占76%。这一比例超过了近年来60%的平均值,也从另一个方面反映了更多EBP公司倾向于独立推动产品上市,而不是授权或出售自主开发的药品。
在中国,由EBP公司研发的NAS在过去的五年中,药物的数量显著增加。报告数据显示,2012-2016年间,上市的83款车型共有83款NAS在药物中,15款最初是从EBP公司开发。2017-2021年,173款上市。NAS在药物中,59款最初是从EBP公司开发。
总的来说,在过去的五年里,EBP公司最初开发或推动上市NAS药品更容易获得FDA这些数据表明,从监管的角度来看,用于加快新药审评的资格认定,EBP与其他公司相比,公司并不处于劣势。
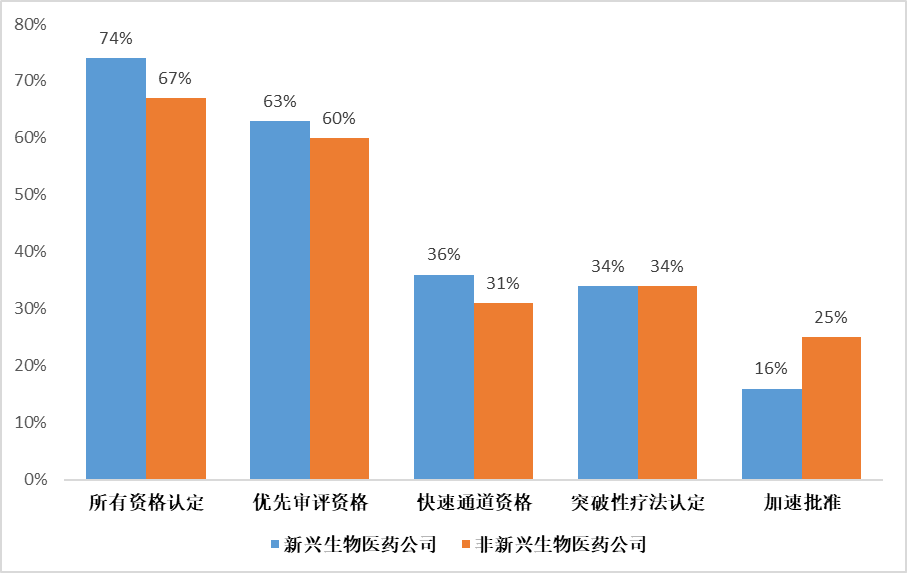
▲2017-2021年上市的NAS药物的FDA资格特征(资料来源:参考资料[1],医药康德内容团队制图)
在美国,EBP公司之所以能够独立推动产品上市,部分原因是其产品具有不同的特点。报告指出,在过去五年中,EBP产品的“first-in-class平均比例为45%,非EBP产品这个值是35%。EBP公司最初开发的平均55%的产品是孤儿药,而不是EBP这一比例的产品是46%。这些特点使得较小的公司能够为患者数量较少的特定群体开发创新疗法,并在一定程度上减少推出产品和商业化所需的资源压力。
结语
如今,人们对健康的需求越来越高,对医疗卫生行业的期望也越来越高。如何支持创新,提高药物研发效率是医疗卫生生态系统中每个成员都需要面对的问题。IQVIA报告显示,新兴制药公司为创新疗法的临床发展和产品的最终上市做出了重要贡献。IQVIA该报告还评估了许多因素,如新兴生物医学公司主导的临床试验特征以及推出产品的创新特征。由于篇幅有限,本文不会逐一详细描述。点击文章末尾的阅读全文/Read more,即可访问IQVIA网站浏览英文全文报告。
参考资料:
[1] Emerging Biopharma’s Contribution to Innovation. Retrieved June 17,2022,from https://www.iqvia.com/-/media/iqvia/pdfs/institute-reports/emerging-biopharma-contribution-to-innovation/iqvia-institute-emerging-biopharmas-contribution-to-innovation-forweb.pdf?utm_medium=email
