迈威生物申报PD-L1/TGF-β RII双功能蛋白
发布时间: 2022-06-17 19:40:18
6月17日,迈威生物6MW国家食品药品监督管理局受理了3511注射液临床试验申请,拟用于治疗各种晚期实体瘤。
6MW3511是迈威生物利用的人源化PD-L1纳米抗体连接TGF-β RII双功能基团药物蛋白是由突变体独立构成的。突变体的设计有助于保持全分子的稳定性,降低自然性TGF-β RII基团在生产过程和体内的降解。同时通过阻断PD-1/PD-L1和TGF-β/TGF-β-R双通道,结构简单带来的优异局部肿瘤穿透力,6MW有望进一步解决肿瘤微环境免疫抑制问题。
临床前研究结果显示MW3511注射液具有良好的抗肿瘤作用和动物耐受性。
国内开发PDL1/TGF-βR还有乐普生物、恒瑞、齐鲁、普米斯等。
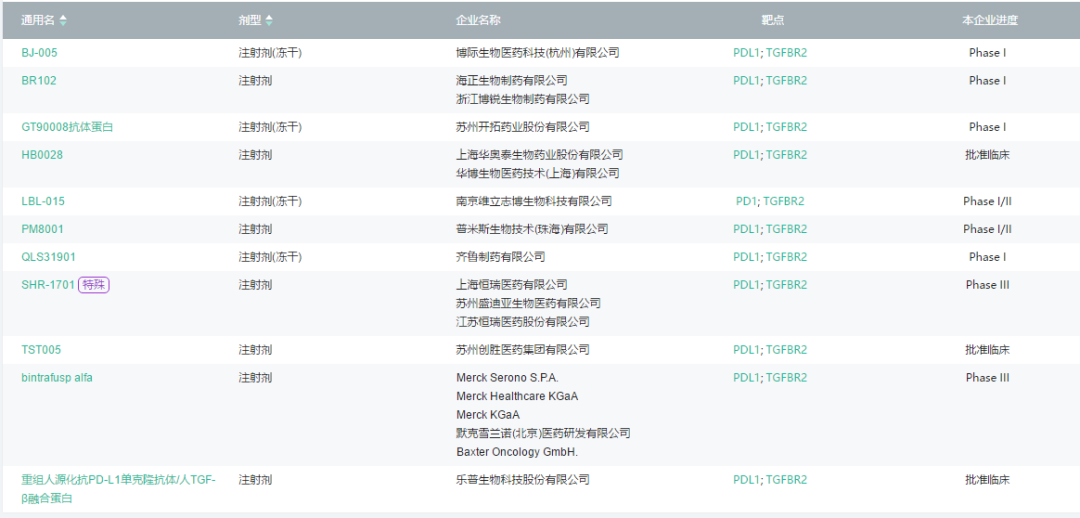
默克的M7824是一款firsit-in-class的PD-L1/TGF-β双功能融合蛋白I这项研究显示了令人兴奋的临床数据。然而,在推进到临床后期M7824多次失败。去年9月30日,GSK关于默克的终止M7824的合作。

