抗流感新药玛巴洛沙韦重拳出击,症状改善效果显著!
发布时间: 2022-06-12 13:40:03
流感再现
流感是一种常见的急性呼吸道传染病,可引起严重后果。患者可能有肺炎、支气管炎和鼻窦炎等并发症,导致住院甚至死亡,这对公众健康构成重大威胁。WHO数据显示,在全球范围内,每年约有5%-10%的成人感染流感,20%-30%的儿童感染,导致重症病例500万例,死亡病例65万例。根据新冠肺炎疫情前的一项研究,中国平均每年有80%.8万例流感相关呼吸系统疾病死亡人数超过8万例,占呼吸系统疾病死亡人数的8%.2%。感染流感的患者,应及时、有针对性地进行抗病毒治疗。
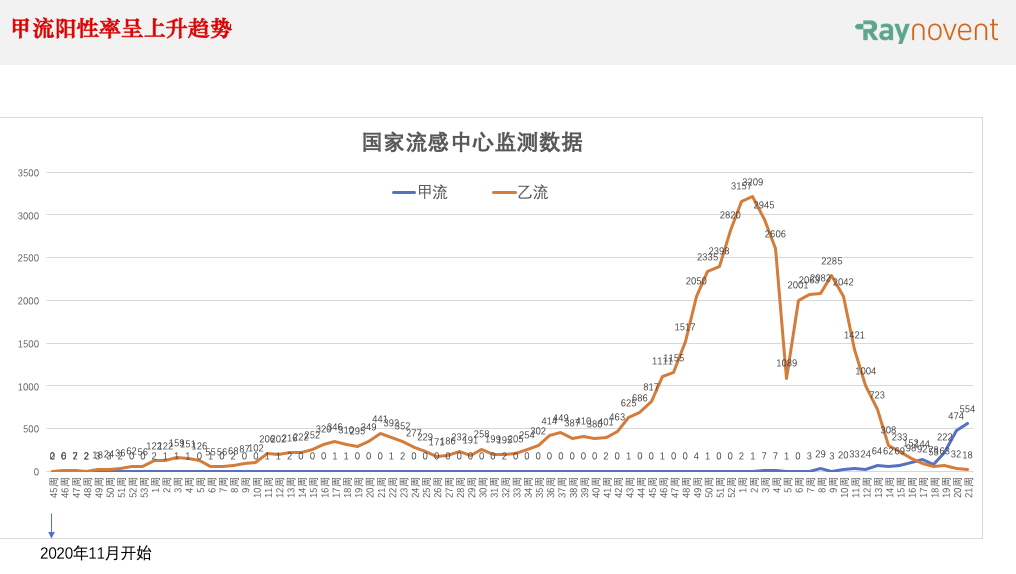
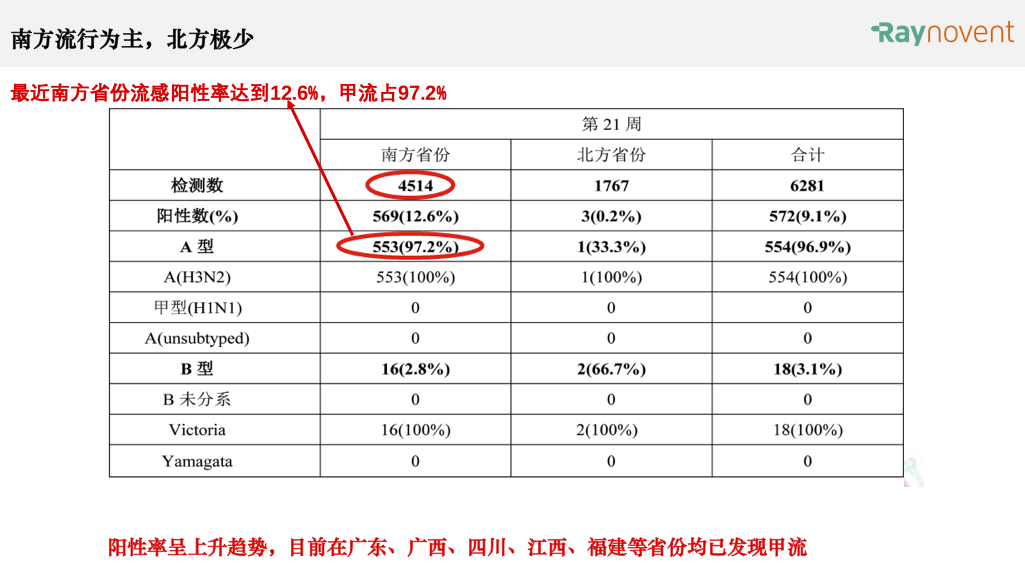
国家流感中心近期数据(2022年第21周),甲流为主
玛巴洛沙韦
罗氏流感创新药速福达2021年4月27日?(英文商品名:Xofluza?,玛巴洛沙韦,英文名:Baloxavir marboxil)中国国家药品监督管理局(NMPA)正式批准用于治疗12岁及以上无并发症的流感患者,包括有高风险流感并发症的患者。(国药准字HJ20100027,国药准字HJ20210028)
【通用名】:玛巴洛沙韦片】
【规格】:20mg*2片/盒
【零售价】:此前医保谈判前为498元;经过医保谈判,目前的价格是2222.36元,每件约111元
核酸内切酶抑制剂是一种创新的帽状结构依赖性核酸内切酶抑制剂(Cap-dependent endonuclease inhibitor),它的作用机制不同于现有的抗病毒疗法。它可以阻断病毒细胞中的核酸内切酶,使病毒失去自我复制的能力。玛巴洛沙韦是第一个也是唯一一种被批准用于治疗流感的口服药物。(Baloxavir marboxil日本盐野义最早(Shionogi)开发;目前,盐野义负责盐野义Xofluza日本市场;罗氏负责;Xofluza开发和销售美国、中国等市场;WO-2010147068、WO-2012039414、WO-2016175224、WO-2018030463)
基本信息:玛巴洛沙韦

截图来源:药融云数据全球药物研发数据库
感染流感的健康人群(CAPSTONE-1临床实验,无基础疾病人群)和流感并发症高危人群(CAPSTONE-2.临床实验)是治疗流感的有效方法。在以前健康的急性无并发症流感患者中CAPSTONE-1.临床实验数据显示,玛巴洛沙韦在既往健康患者中有效且具有良好的耐受性。与安慰剂相比,服用玛巴洛沙韦的患者的症状改善时间可以缩短26.5小时(安慰剂80).2h vs玛巴洛沙韦53.7h),退热时间可以缩短17.5小时(42)安慰剂h vs玛巴洛沙韦24.5h )。高危流感并发症患者进行的CAPSTONE-在临床实验中,玛巴洛沙韦也表现出有效性,可以减少并发症的发生。与安慰剂相比,服用玛巴洛沙韦的高危患者的症状改善时间可以缩短29.1小时(安慰剂102).3h vs玛巴洛沙韦73.2h)。
之前是2021年77CDE接受石药石药欧意提交 4 类仿制药玛巴洛沙韦片上市申请。本品是国内首家申报上市的仿制药。
玛巴洛沙韦电影国内上市申报
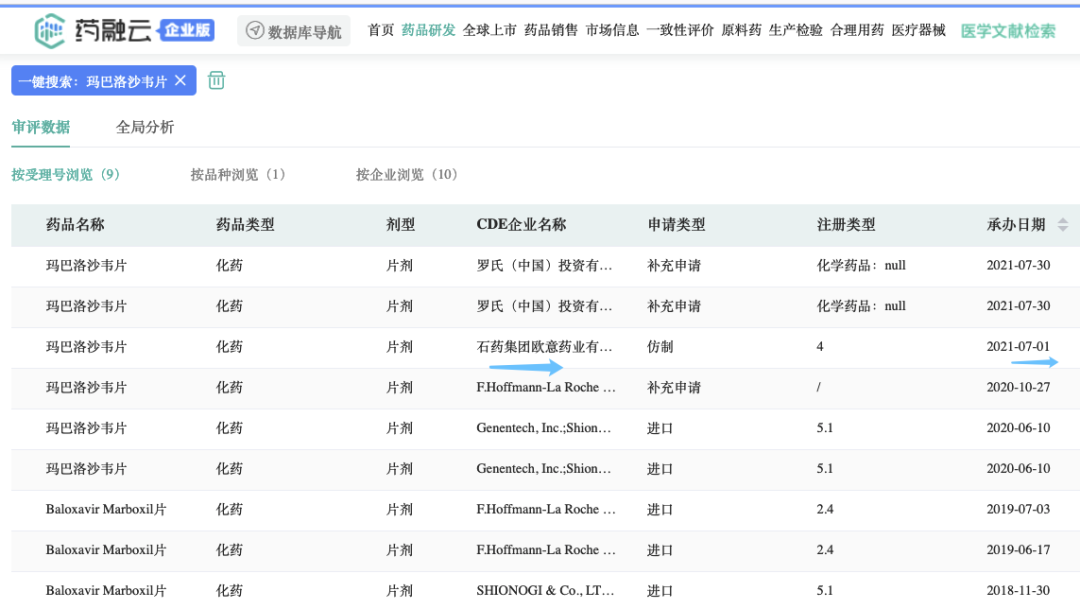
截图来源:药品融云数据中国药品评价数据库
正在研究国内流感新药
根据药融圈和药融云数据,目前国内流感新药正在研究的企业有:众生瑞创ZSP1273片及颗粒,珍宝岛药业/广州恒诺康药业HNC042、青峰医药/银杏树GP681.太景医药研发(北京)有限公司TG-1000、征祥药抗流感新药ZX-7101A、安帝康生物ADC189和中国药科大学抗病毒新药黄芩素(天然药物衍生);除了流感疫苗(包括热疫苗)mRNA除了疫苗),许多流感领域的小分子新药都处于临床前研究阶段(如圣诺制药/沃森生物siRNA()

广东中盛瑞创生物科技有限公司:预防甲型流感和禽流感RNA一类创新药物的聚合酶抑制剂ZSP1273片正在积极开展三期临床试验,目前已有多例入组(2022年5月15日公告:首例单纯性甲型流感患者入组)。
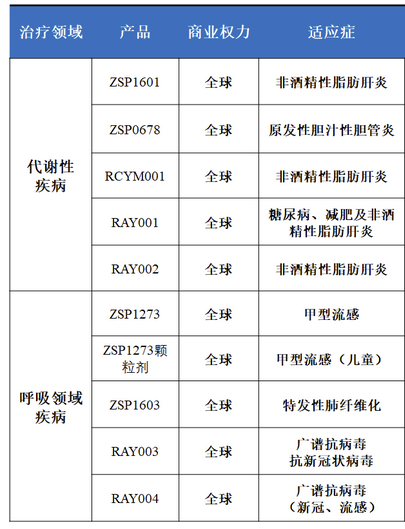
pipeline,www.raynovent.com/ray/science.html
安迪康(无锡)生物科技有限公司自主研发的新药,用于治疗和预防甲型和乙型流感ADC189临床试验申请(IND),此前,他被中国国家药品监督管理局药品审评中心授予(CDE)默示许可。ADC189具有全新的抗流感机制,可直接抑制病毒的复制。Cap通过抑制流感病毒中的流感病毒,依赖型核酸内切酶抑制剂CAP帽子结构依赖性内切核酸酶。安迪康生物对ADC189的设计和开发旨在对抗甲型和乙型流感病毒,包括对抗奥司他韦(oseltamivir)耐药流感株和禽流感株(H7N9,H5N1)。
ZX-7101A是新一代征祥医药完全自主研发的新一代PA抑制剂具有广谱抗流感的特点,对甲、乙型流感病毒和高致死性禽流感病毒具有优越的活性。目前,已批准进行临床试验。临床前研究表明,ZX-7101A与此同时,抗病毒明显优于奥司他韦,ZX-7101A口服生物利用率较高,无食物效应问题,进一步提高了安全性和有效性。
参考:
NMPA/CDE;
药融云数据https://www.pharnexcloud.com/?zmt-xlyy;
FDA/EMA;
公开披露相关公司;
CDE关于公开征求《流感抗病毒药物临床试验技术指导原则(征求意见稿)》的通知;
安帝康生物;等等。
