罗氏公布了肿瘤学研发管道的最新进展
日前,罗氏的CD20/CD3 T细胞连接双特异性抗体Lunsumio(mosunetuzumab)获得欧盟有条件上市批准,成为世界上第一个获得监管机构批准的CD20/CD3双特异性抗体。罗氏在抗体工程改造领域有着悠久的历史。目前,该公司已批准上市三种双特异性抗体,最近在市场上ASCO在年会期间举行的投资者活动中,该公司详细介绍了其肿瘤研发管道。它不仅包括许多双特异性抗体,还包括许多早期研发项目,从靶向免疫系统到直接靶向肿瘤细胞,使用各种治疗模式来对抗癌症,可以说是充满了干货。
罗氏肿瘤管道主要分为两类,一类是癌症免疫治疗,另一类是癌细胞靶向治疗。这两种类型都使用多种治疗模式来开发新药。
在癌症免疫疗法中,罗氏的一个重要方向是使用双特异性抗体对抗癌症T细胞被重新定位,并被招募到表达特定抗原的肿瘤细胞周围,以发挥其杀伤作用。刚刚获得批准的Lunsumio另外,公司开发的glofitamab也进入了三期临床开发阶段。这个模型。T两个细胞连接双特异性抗体可以携带CD20组合的蛋白质域和一个可以和CD蛋白质结合。
在ASCO年会上公布的关键第二阶段临床试验的最新结果表明,在高度难治性弥漫性的治疗中B细胞淋巴瘤(DLBCL)中位随访时间为12.6个月时,39.4%的患者获得完全缓解,总缓解率为51.6%。值得一提的是,之前已经接受了CAR-T治疗病人,glofitamab也表现出一致的完全缓解率。
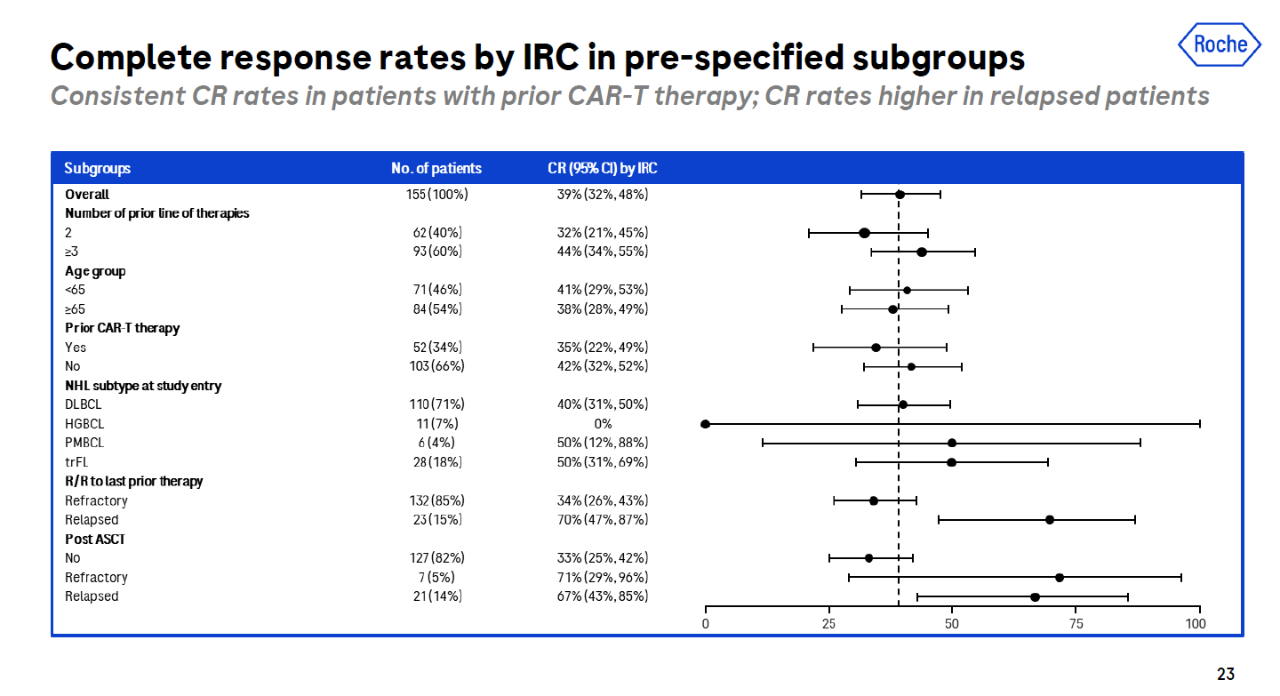
▲Glofitamab不同亚群患者的完全缓解率(图片来源:罗氏官网)
Glofitamab疗效持久,12个月的缓解持续率为63.6%,在获得完全缓解的患者中,12个月完全缓解的持续率为77.6%。在接受早期治疗的患者队列中,24个月的完全缓解持续率达到61.4%。
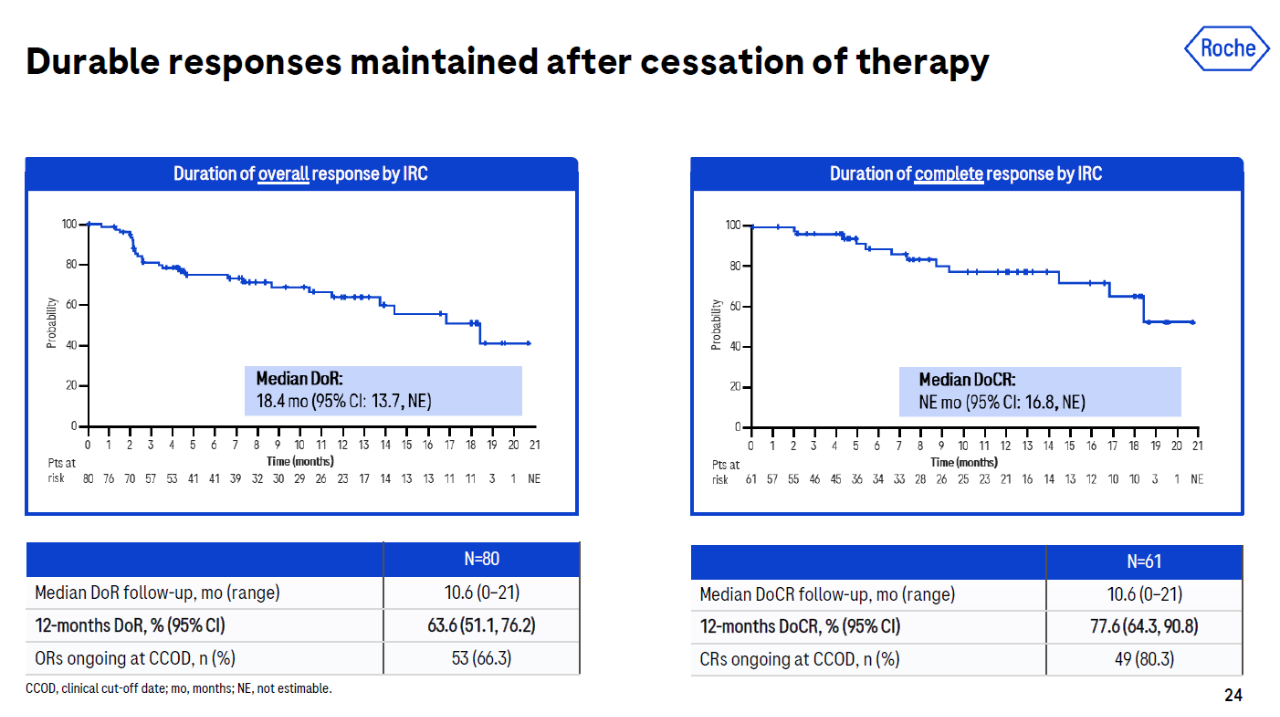
▲Glofitamab带来持久缓解(图片来源:罗氏官网)
在投资者会议上,罗氏还介绍了其他重新定位T双特异性抗体治疗。
RG6234:潜在“best-in-class”GPRC5D/CD双特异性抗体
RG6234是一个靶向新兴目标GPRC5D的T细胞连接双特异性抗体。它携带两个靶向抗体GPRC5D蛋白质域和靶向CD3的蛋白域。GPRC5D它是多发性骨髓瘤表达的高特异性蛋白。罗氏说,这种双特异性抗体具有best-in-class潜力。在治疗复发性/难治性多发性骨髓瘤患者的早期临床试验中,客观缓解率为68%,部分缓解率超过50%。
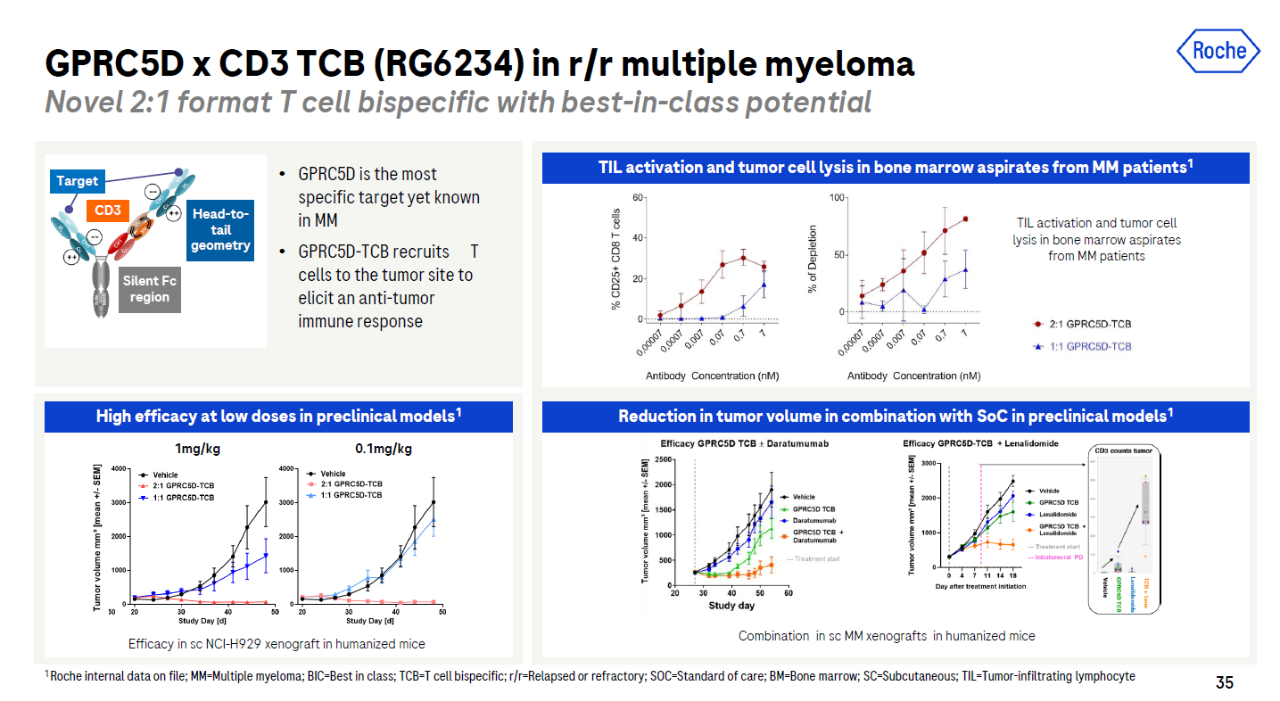
▲RG6234简介(图片来源:罗氏官网)
RG6007:模拟TCR双特异性受体抗体
罗氏的RG6007是一款与TCR具有类似受体的双特异性抗体,可以靶向从HLA-A2细胞中的致癌蛋白WT1片段,并激活T细胞的CD受体3。它是基于急性髓系白血病的(AML)在体外实验和小鼠模型中,患者的血液样本表现出良好的活性,目前正在进行一期临床试验。
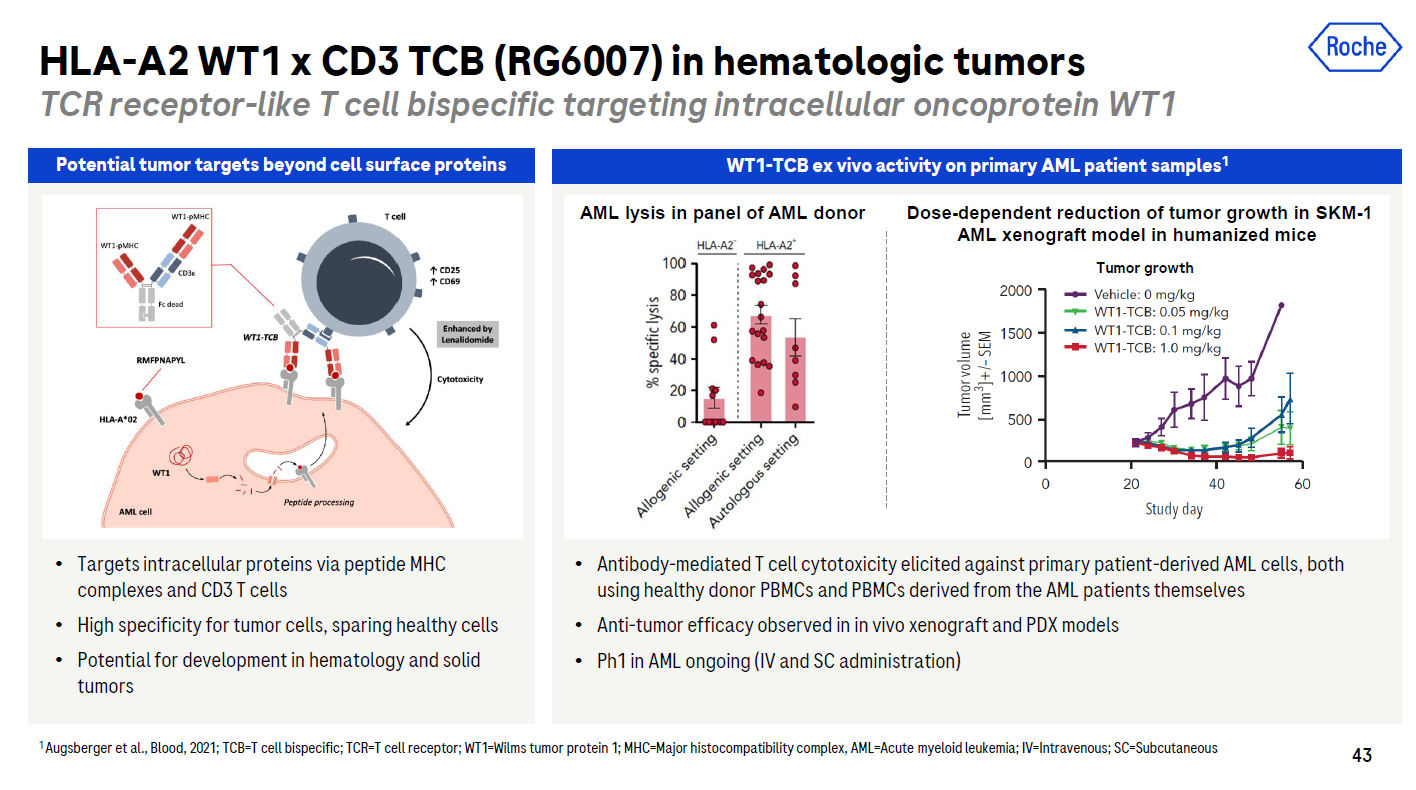
▲RG6007简介(图片来源:罗氏官网)
除了重新定位T细胞、罗氏开发的双特异性抗体也可以通过其他多种机制进行调节T细胞活性。
RG6076:增强T共同刺激受体的细胞功能
RG6076是由靶向CD蛋白质域和靶向19T4-1BB双特异性抗体由配体融合形成。它可以靶向激活B细胞附近T4-1BB。与CD20/CD3 T双特异性抗体的细胞连接可以进一步增强T细胞功能。目前,它正处于第一阶段临床试验中glofitamab用于治疗复发/难治性非霍奇金淋巴瘤(r/r NHL)患者。
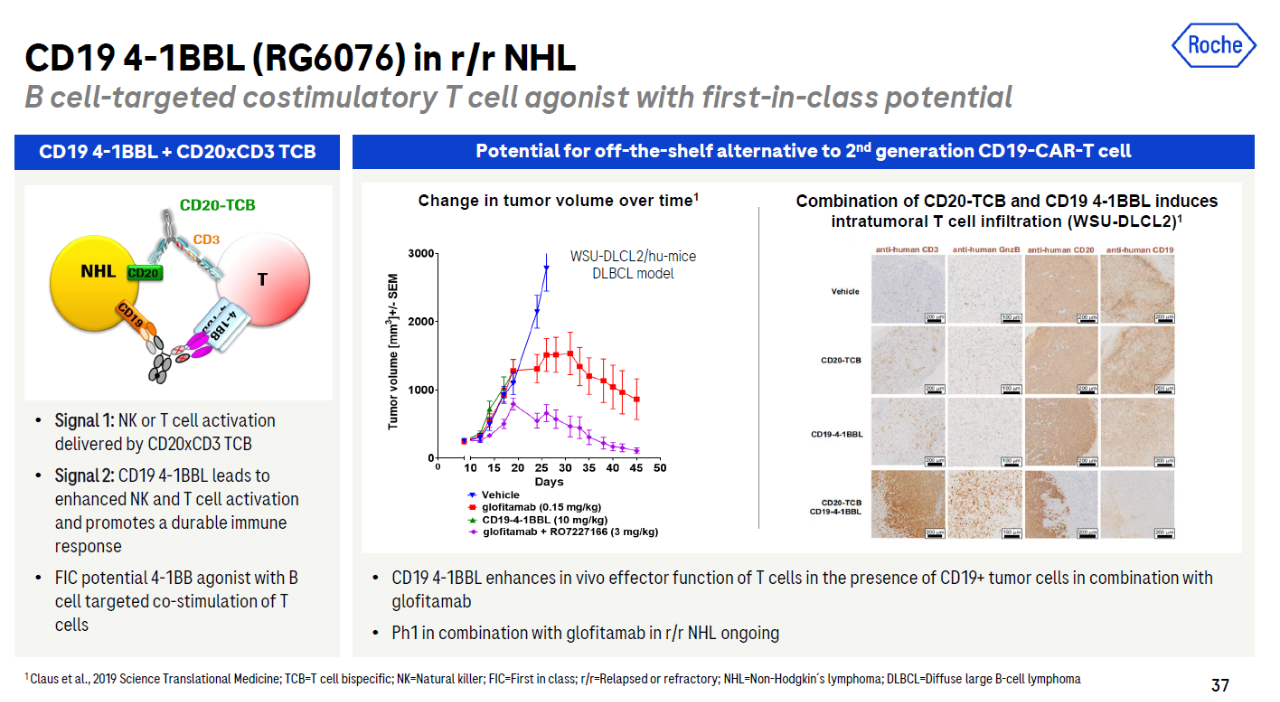
▲RG6076简介(图片来源:罗氏官网)
RG6333:T细胞刺激受体激动剂
RG6333将靶向CD19蛋白质域和激活共同刺激受体CD28的蛋白质域连接在一起。它与上面提到的相连RG与小鼠模型相比,6076具有不同的机制。CD20/CD3 T细胞连接的双特异性抗体组合表现出更强的表现T细胞活性。目前,也在一期临床试验中glofitamab联用,治疗r/r NHL患者。
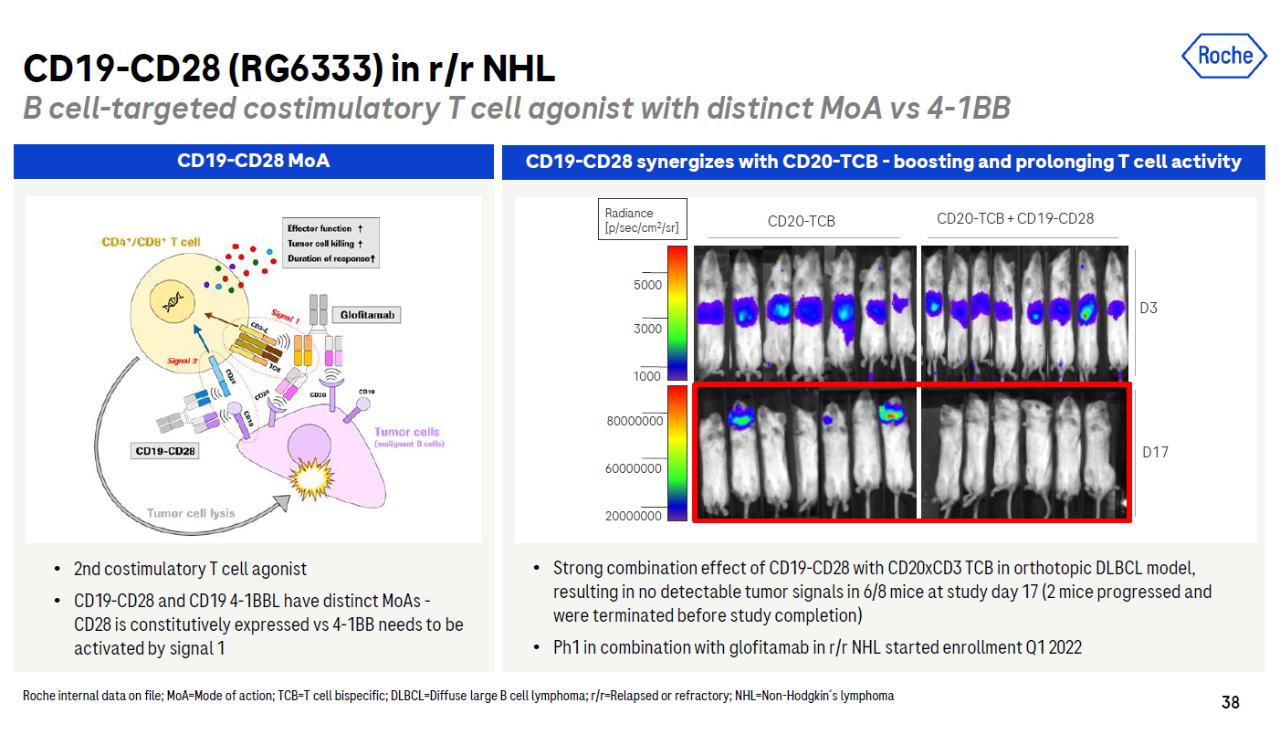
▲RG6333简介(图片来源:罗氏官网)
RG6139:双特异性免疫检查点抑制剂优先靶向肿瘤浸润淋巴细胞
RG6139是一款靶向PD-1和LAG-3同时阻断双特异性抗体PD-1和LAG-3.激活介导的检查点信号通路,T细胞的抗癌反应。它可以优先考虑肿瘤浸润淋巴细胞的肿瘤反应(TIL),减少和调节T避免免疫抑制作用的细胞结合。
它已经完成了一期临床试验,用于实体瘤患者的剂量搜索。目前在1b治疗食管癌、肝细胞癌和黑色素瘤的/2期研究。
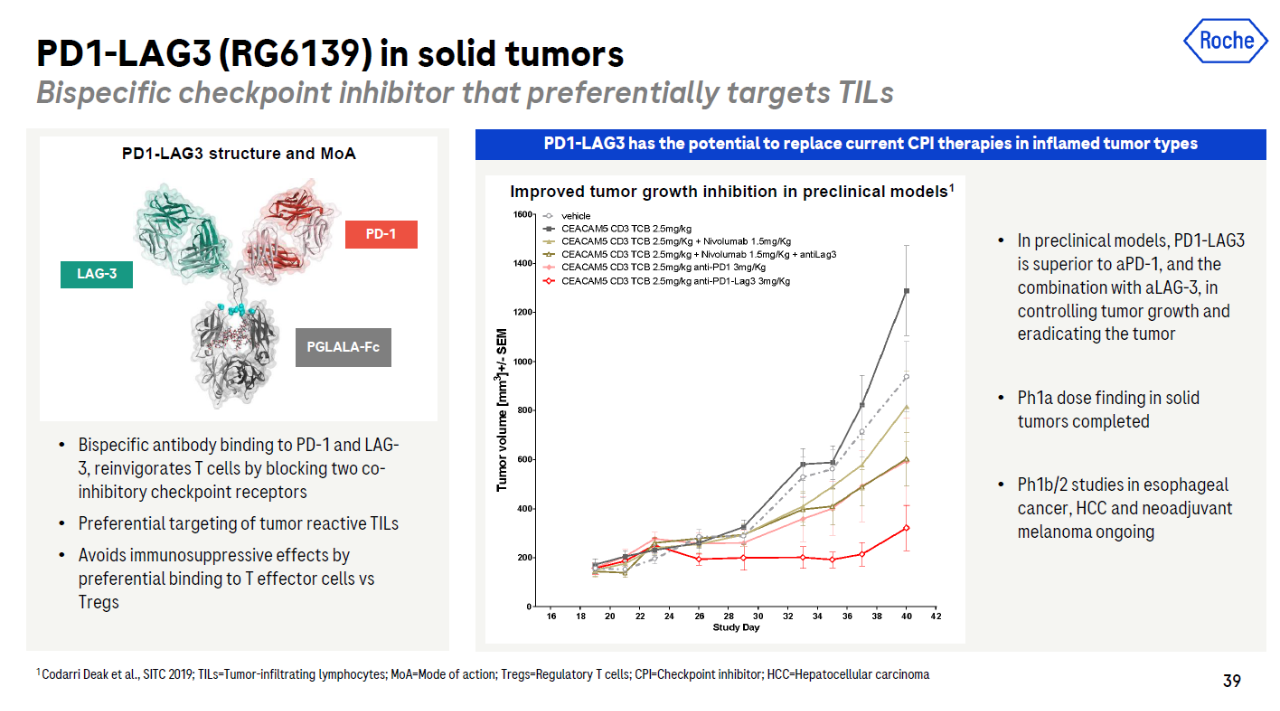
▲RG图片来源:罗氏官网)
RG6279:靶向递送IL-2变体
名为RG6279的抗PD-1抗体具有独特的结构,其结构Fc添加了一个IL-2变体。这个IL-2.变体的设计消除了它IL-2Rα(又名CD25)结合的能力,从而避免了它与内皮细胞的结合,消除了调节性T细胞(Treg)扩增的作用。它可以具有特异性IL-2变体送到表达式PD-1的T细胞附近,传统PD-与抗体相比,抗体能更有效地刺激细胞毒性作用T细胞扩增。罗氏说,这是第一个进入临床开发阶段的PD-1靶向免疫细胞因子疗法。
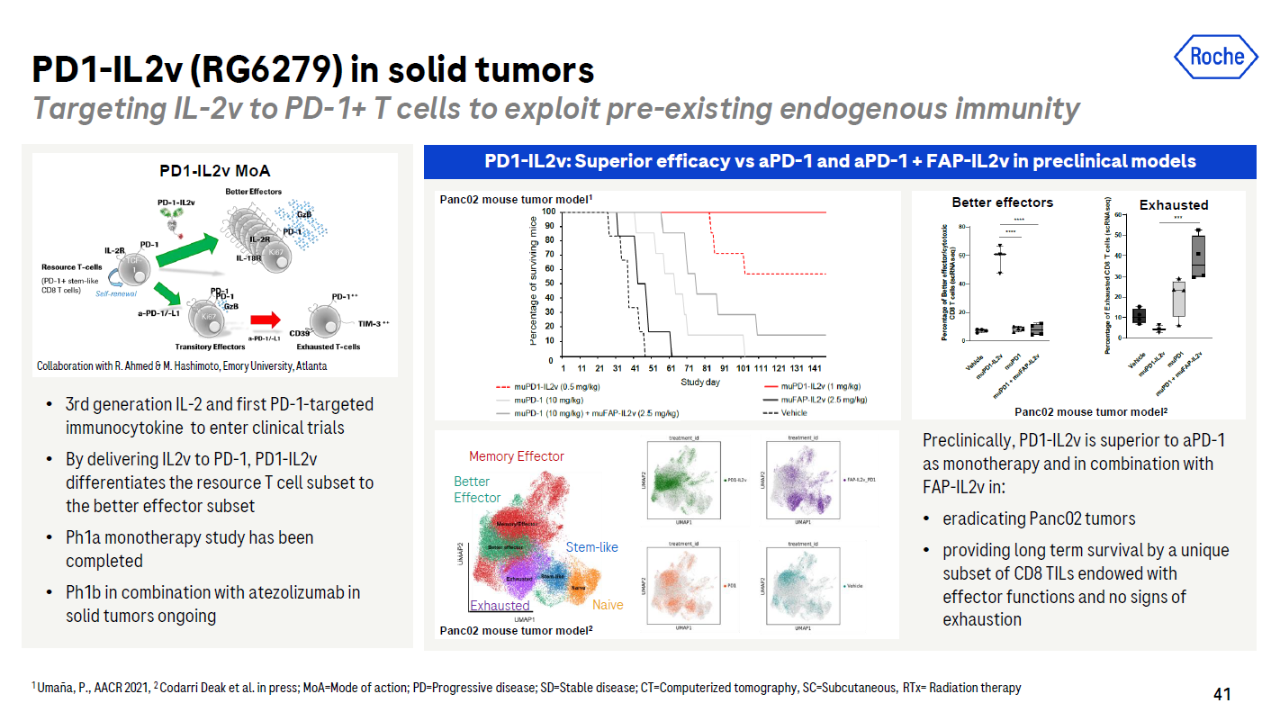
▲RG图片来源:罗氏官网)
RG6189:靶向激活抗原呈递细胞
RG6189可用于肿瘤基质环境FAP在蛋白质存在的情况下CD40共同刺激受体并激活其信号通路。这对特异性抗体可以激活抗原来表示细胞(APC),增强肿瘤特异性抗原。它具有非常高的肿瘤特异性,因此可以避免第一代CD40激动剂潜在的全身毒副作用,并增加剂量。
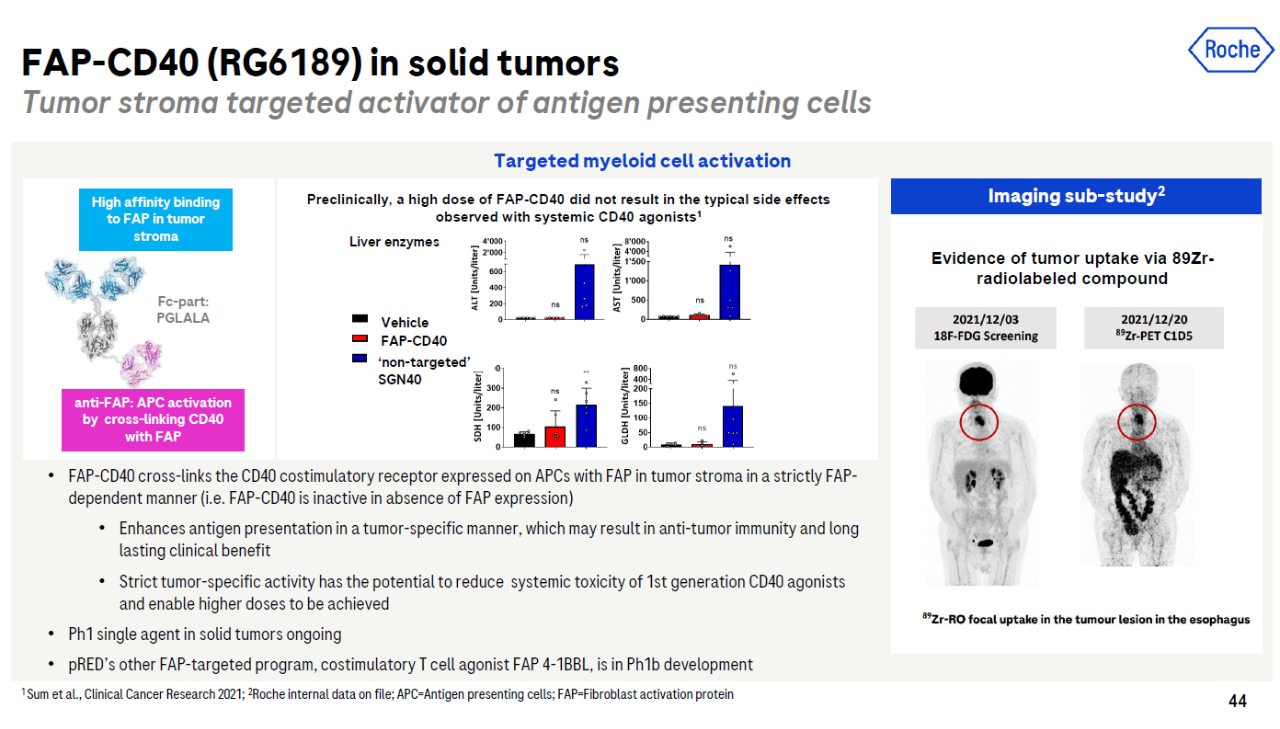
▲RG图片来源:罗氏官网)
除了使用双特异性抗体来调节抗癌免疫反应外,罗氏还与Chugai Pharmaceutical公司与失活状态合作开发TGF-β1结合的抗体SOF10(又名RG6440)。TGF-β1是抑制肿瘤微环境的关键调节因子之一T细胞浸润起着重要作用。处于失活状态TGF-β激活蛋白酶切割或整合素,SOF10通过和失活TGF-β防止其激活,从而重塑肿瘤微环境,促进淋巴细胞的渗透。
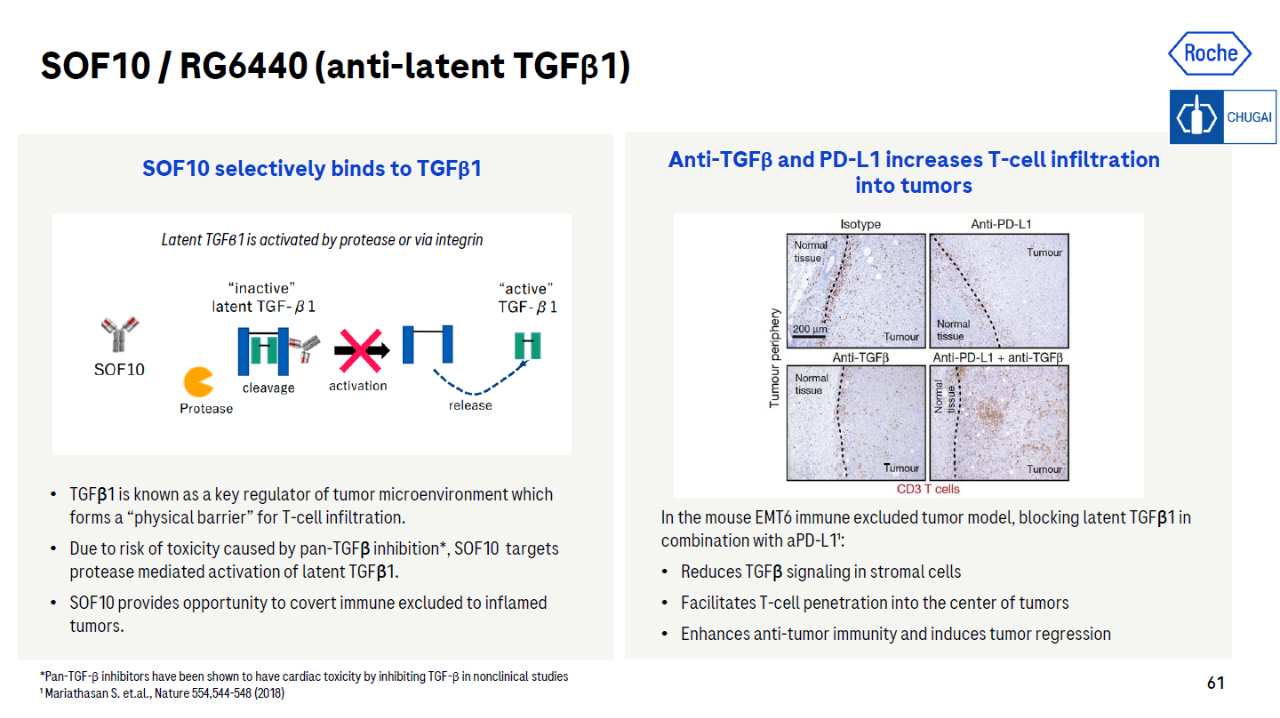
▲SOF10/RG6440简介(图片来源:罗氏官网)
罗氏抗癌药物开发的另一个主要方向是靶向致癌信号通路。该公司有许多从不同角度进行靶向治疗的研究方法RAS-MAPK信号通路。
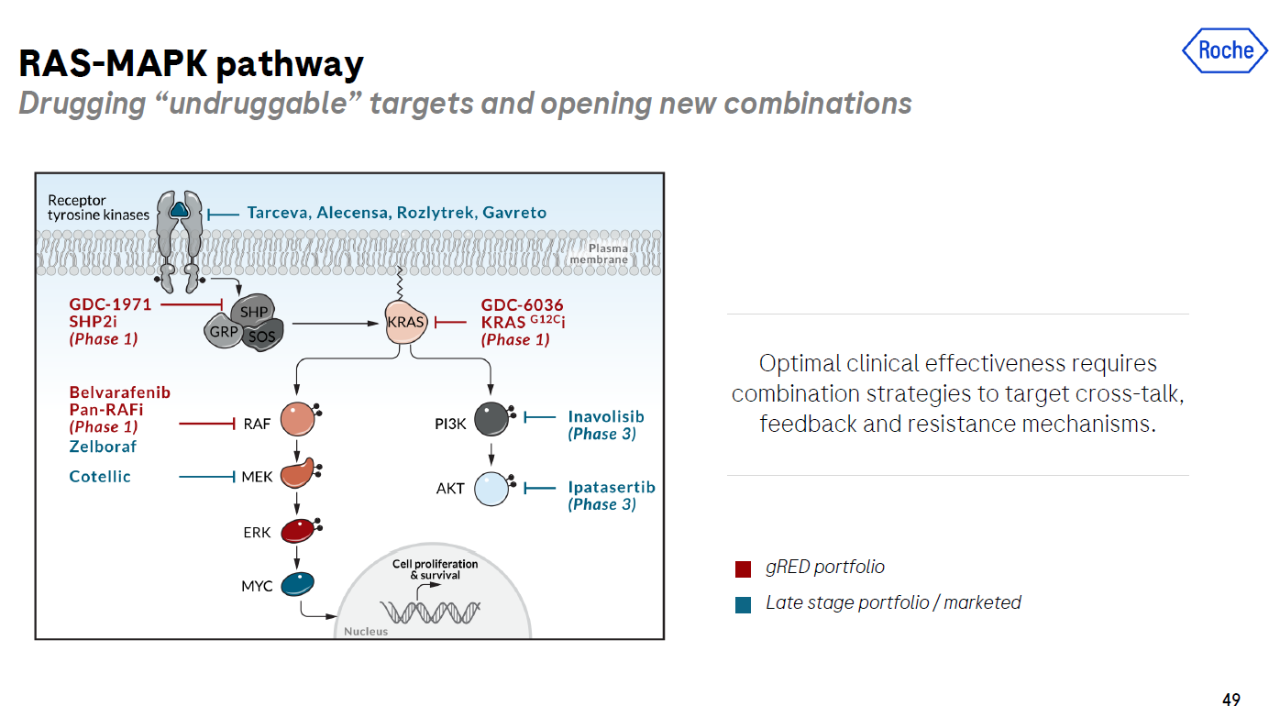
▲罗氏靶向RAS-MAPK信号通路(图片来源:罗氏官网)的多种审批和研究疗法
其中,GDC-6036是不可逆的KRAS G12C可以使用共价抑制剂KRAS G12C锁定在失活的构象中。在临床前研究中,罗氏表示,它表示best-in-class”的潜力。
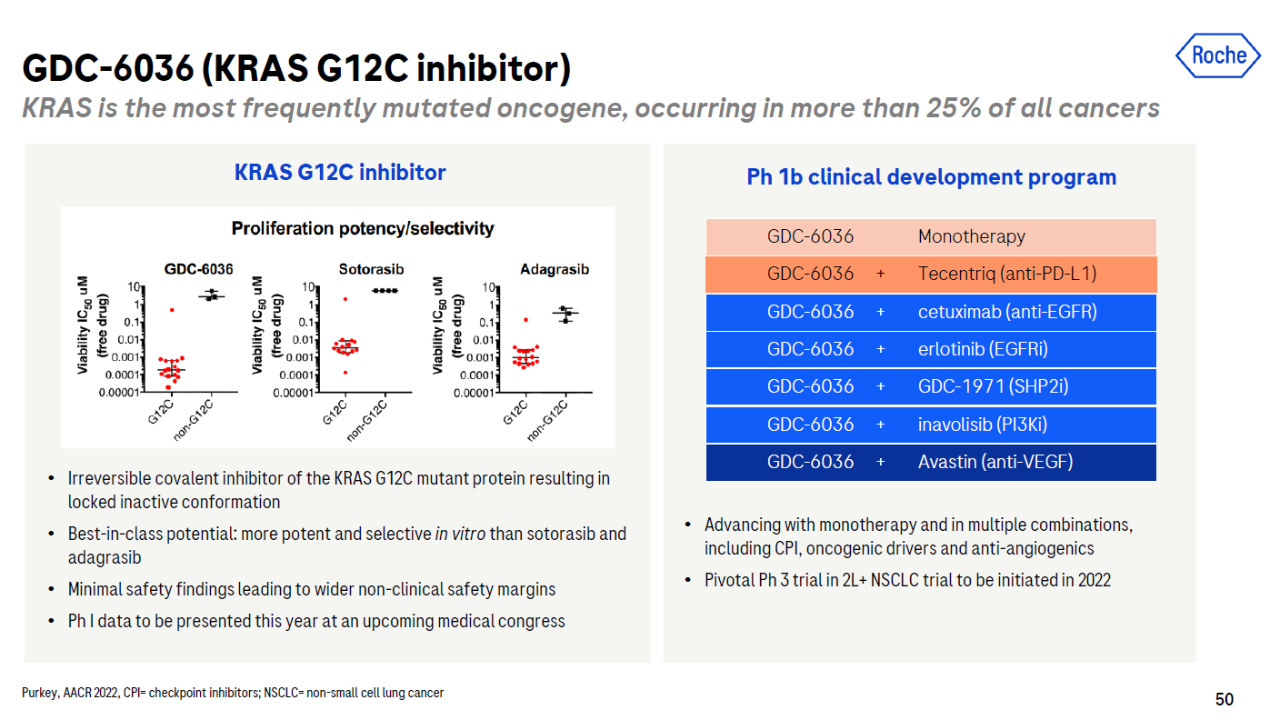
▲GDC-6036简介(图片来源:罗氏官网)
GDC-1971是一种口服选择性SHP2抑制剂,它与KRAS G12C抑制剂联合,在临床前模型中表现出协同作用。
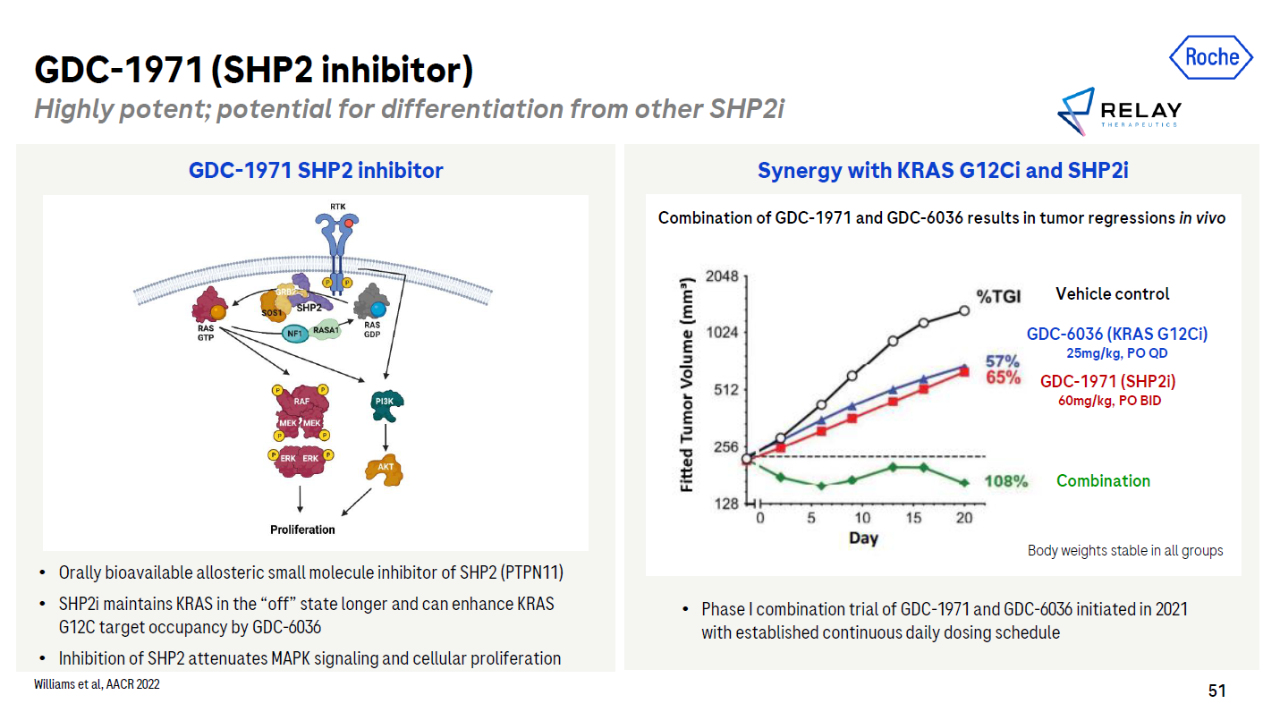
▲GDC-图片来源:罗氏官网)
罗氏还介绍了该公司BioNTech基于联合开发mRNA新抗原癌疫苗在技术平台上的最新进展。这个结果已经在了ASCO年会发布。
参考资料:
[1] ASCO 2022 Virtual IR event. Retrieved June 9,2022,from https://assets.cwp.roche.com/f/126832/x/2adb205911/ir-asco-2022-event.pdf
