获得放射性抗体疗法FDA治疗神经母细胞瘤的优先资格
今日,Y-mAbs Therapeutics公司宣布,FDA该公司在研究中授予疗法Omblastys(omburtamab)申请生物制品许可(BLA)中枢神经系统/软脑膜转移瘤用于治疗儿科神经母细胞瘤患者。Omburtamab这是一种针对肿瘤抗原的放射性碘标记抗体疗法B7-H3。FDA预计在今年11月30日之前做出回应。
Omburtamab纪念斯隆-凯特琳癌症中心(MSK)开发研究人员,Y-mAbs Therapeutics获得其独家开发权益。B7-H它是一种蛋白质,表达在神经母细胞瘤和瘤表面的蛋白质。放射性标记omburtamab可直接注射到儿童脑室,使药物能接触到大脑肿瘤。
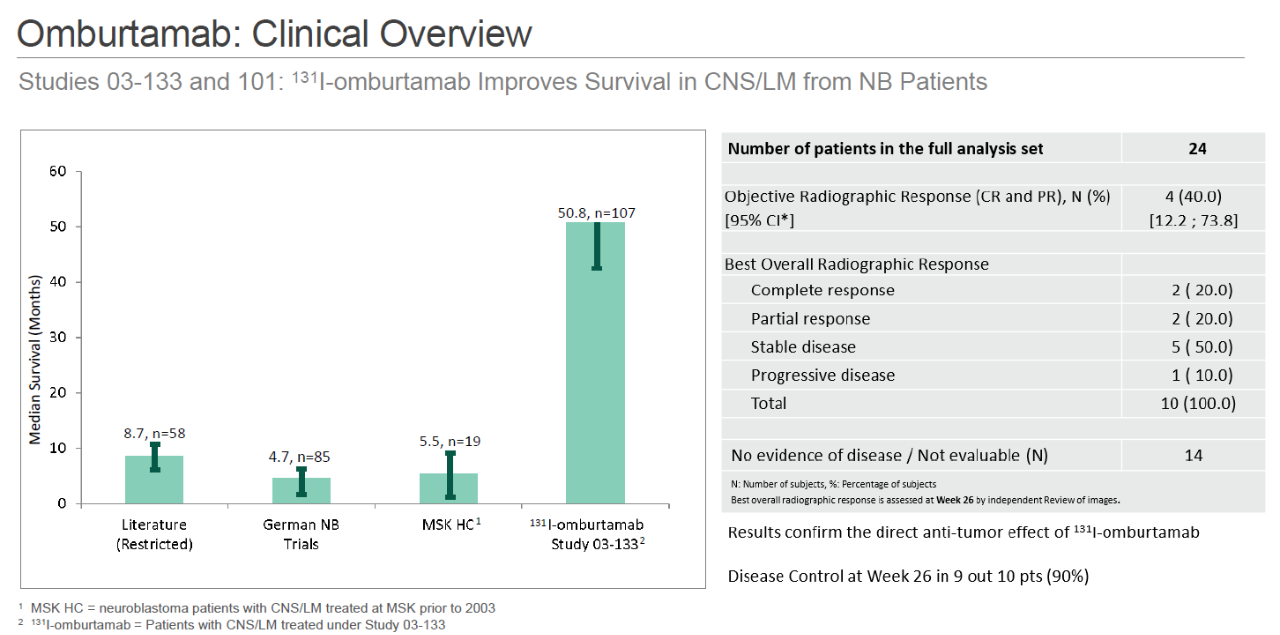
这一BLA这是基于关键性二期临床试验的安全性和有效性结果。Y-mAbs根据官网公布的结果,在接受治疗26周的10名儿童中,疾病控制率达到90%,其中部分缓解2人,完全缓解2人。
图片来源:Y-mAbs官网
我们相信,FDA授予Omblastys的BLA优先审查资格是一项重要进展。如果获得FDA预计中枢神经系统/脑膜转移瘤患儿的医疗需求将得到解决,目前没有标准治疗。Y-mAbs临时总裁兼首席执行官Thomas Gad先生说:我们期待和FDA合作,早日将Omblastys把它带给合适的孩子。
参考资料:
[1] Y-mAbs Announces FDA Acceptance of Biologics License Application for OMBLASTYS? (omburtamab) for the Treatment of Neuroblastoma for Priority Review. Retrieved May 31,2022,from https://www.globenewswire.com/news-release202/2/2/2/2/2/2/2/2/2/2/2/2/2/2/2/2/1/2/2/2/2/2/2/2/2/2/2/2/2/2/2/2/2/2/2/1/2/2/2/2/2/1/2/2/2/2/2/2/1/2/2/2/2/2/2/2/2/2/2/2/2/2/2/2/2/2/1/2/2/2/2/2/2/2/2/2/2/1/2/2/1/2/2/2/1/2/2/2/1/2/2/2/2/2/1/2/2/2/2/1/2/1/2/2/2/1/2/1/2/1/2/1/2/1/2/1/2/1/2/1/2/2/1/2/2/2/1/2/2/1/2/2/1/2/2/2/1/2/2/1/2/2/1/2/1/2/1/2/1/2/1/2/2/1/2/2/2/1/2/2/2/1/2/2/2/2/1/2/1/2/2/2/1/2/1/2/2/2/2/1/2/2/1/1/1/1/2/2/2/2/2/2/2/1/1/2/1/2/2/2/1/1/1/1/1/1/2/2/2/2/2/2/2/2/2/2/2/2/2/2/1/1/2/2/2/2/2/1/1/1/1/2/2/2/2/2/2/2/2/2/2/2/2/2/2/2/2/2/2/2/2/2/1/1/1/1/1/2/2/2/2/1/2/2/2/1/1/1/1/1/1/1/2/1/1/1/2/2/2/1/1/1/1/1/1/2/1/1/1/2/1/1/1/1/1/1/1/1/en/Y-mAbs-Announces-FDA-Acceptance-of-Biologics-License-Application-for-OMBLASTYS-omburtamab-for-the-Treatment-of-Neuroblastoma-for-Priority-Review.html
