Nature综述 | 恶性黑色素瘤市场格局:预计2030年销售额为72亿美元
文章来源:医药魔方Pro
作者:白露
恶性黑色素瘤是一种起源于皮肤黑色素细胞的肿瘤,恶性程度高,是第三种常见的皮肤癌,被认为是皮肤癌相关死亡的主要原因。局部和远端转移性黑色素瘤(分别是III期和IV期)预后不同,但通常很差,III五年生存率为13%~69%,IV期低至6%。
随着免疫治疗的兴起,特别是免疫检查点抑制剂的应用,晚期黑色素瘤患者的生存期显著延长。未来,基于免疫检查点抑制剂的治疗模式将逐步改善恶性黑色素瘤患者的生存。
4月27日,Nature Reviews Drug Discovery本文从当前治疗、新兴治疗和市场指标三个维度分析了恶性黑色素瘤市场:免疫检查点将继续占据主导地位,联合治疗将逐步增加。
当前疗法
在过去的10年里,PD-1/PD-L1免疫检查点抑制剂、小分子BRAF和MEK抑制剂和包含这些药物的联合方案创新了恶性黑色素瘤的治疗。
约40%~50%的恶性黑色素瘤患者表达BRAFV600激活突变BRAF/MEK抑制剂联合疗法已被批准用于治疗BRAFV600突变阳性不可切除或转移性黑色素瘤患者。它们是:维莫非尼 考比替尼(Zelboraf Cotellic;罗氏/基因泰克/日本中外制药)(Tafinlar Mekinist;诺华);恩可非尼 比尼替尼尼替尼(Braftovi Mektovi;辉瑞)。与单剂相比BRAF抑制剂,它们将优先使用。其中,达拉非尼 曲美替尼也被批准用于。BRAFV600突变阳性淋巴结患者(局部晚期或局部晚期或局部淋巴结患者)III期病)完全切除后的辅助治疗。这是唯一被批准作为辅助治疗的辅助治疗BRAF/MEK抑制剂组合。
PD-1抑制剂纳武利尤单抗(Opdivo;百时美施贵宝)和帕博利珠单抗(Keytruda;默沙东)在各种癌症治疗模式中确立了坚实的地位。它们的适应症标签广泛,涵盖了不可切除的转移性癌症的治疗,以及淋巴结患者的辅助治疗。2021年12月,FDA帕博利珠单抗的标签范围进一步扩大,具有高复发风险的完全切除IIB-C患者包括;纳武利尤单抗在同一条件下进行III期临床试验。
阻断双重免疫检查点,如双重免疫检查点,PD-1抑制剂纳武利特单抗和 CTLA-4 抑制剂伊匹木单抗(Yervoy;百时美施贵宝也被批准用于治疗不可切除或转移性黑色素瘤。这种联合疗法显示了前所未有的6年中位总生存期(OS),不到十年前的生存期只有六九个月。2022年3月,FDA一个靶向被批准LAG-3和PD-1的新型first-in-class免疫检查点抑制剂组合Opdualag(百时美施贵宝)是纳武利尤单抗 relatlimab用于治疗不可切除的转移性恶性黑色素瘤的固定剂量组合。III期试验RELATIVITY-047与纳武利尤单抗单药疗法相比,联合疗法中位无进展生存期(PFS)增加了一倍多,显示出与纳武利尤单抗相似的安全性。Opdualag也正在被评估III-IV黑色素瘤完全切除后的辅助治疗(RELATIVITY-098)。
包含PD-L1阿替利珠单抗抑制剂(Tecentriq;罗氏/基因泰克/日本中外制药)BRAF抑制剂维莫非尼和MEK抑制剂考比替尼的三联疗法是晚期BRAFV600突变阳性患者提供了另一种一线治疗方案。尽管三联疗法处于中位。PFS与响应持续时间比BRAF/MEK二联疗法较长,但缺乏成熟OS数据,而且毒性更高。另一个原因是另一个原因。PD-1抑制剂(帕博利珠单抗)和BRAF/MEK三联疗法由抑制剂(恩可非尼/ 比尼替尼)组成III期 STARBOARD被评为晚期黑色素瘤的一线治疗。
Talimogene laherparepvec(Imlygic;安进)是一种具有持久抗肿瘤活性的局部溶瘤病毒病变治疗。它被批准用于治疗第一次手术后不可切除的皮肤、皮下和淋巴结病变的复发患者。
新兴疗法
研究管道中的恶性黑色素瘤主要包括现有疗法(例如)PD-1抑制剂)和新疗法的组合疗法。详见下表。
表1 | 部分皮肤恶性黑色素瘤在研究和治疗中
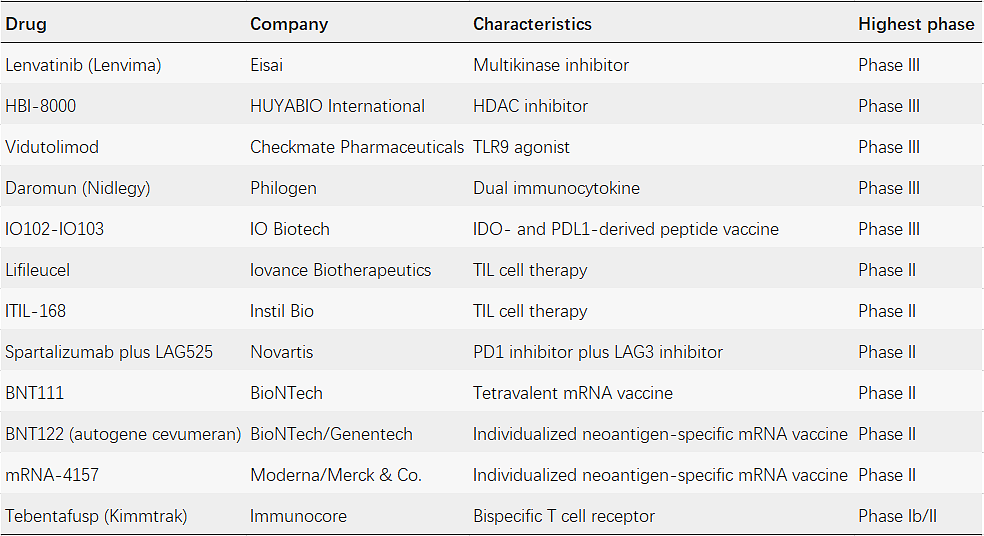
注:HDAC=histone deacetylase; IDO=indoleamine 2,3-dioxygenase; TLR9=toll-like receptor 9(来源:Nature Reviews Drug Discovery)
仑伐替尼(Lenvima;Eisai)它是一种多种酪氨酸激酶抑制剂,与帕博利珠单抗结合在一起III期试验(LEAP-003)被研究为不可切除或转移性黑色素瘤的一线治疗。该疗法仍在进行中。LEAP-004 II在期间试验中,评估用于接受抗抗性试验PD-1/PD-L1治疗后进展的患者,中位患者,中位患者,OS为14个月。
组蛋白去乙酰化酶(HDAC)抑制剂HBI-8000,即西达本胺(Hiyasta;HUYABIO)联合纳武利尤单抗的口服疗法正在进行中III期临床试验用于晚期恶性黑色素瘤患者,他们以前没有接受过免疫检查点的抑制治疗。西达本胺是深圳微芯生物自主研发的具有全新化学结构和全球专利授权的亚型选择性HDAC抑制剂于2014年12月被批准用于治疗复发或难治性外周T细胞淋巴瘤。
处于III临床试验阶段还有两种病变内疗法。第一种是。TLR9激动剂vidutolimod(Checkmate Pharmaceuticals),它以生物病毒样颗粒的形式交付,可以激活先天性免疫系统。该药物正在与纳武利尤单抗联合使用,作为晚期黑色素瘤的一线治疗药物(CMP-001-011),并已获得FDA快速通道资格。二是快速通道资格。daromun(Nidlegy,Philogen),这是一种双重免疫细胞因子组合,包括L19-IL2(darleukin)和L19-TNF(fibromum),靶向纤连蛋白EDB结构域。Daromun被评估为IIIB–C黑色素瘤的新辅助疗法。
一些治疗性疫苗也在进行恶性黑色素瘤的临床试验,它们都与恶性黑色素瘤相结合。PD-1共同使用抑制剂进行评估。其中最领先的是。IO102-IO103(IO Biotech),这是一种基于肽的疫苗,旨在靶向2、3-dioxygenase(IDO)和PD-L1。在III期试验IOB-013/KN-D18中,IO102-IO103联合帕博利珠单抗被评为未经治疗的不可切除或转移性黑色素瘤一线疗法。其他治疗性疫苗是基于mRNA是的,正在进行中II期试验。BNT111(BioNTech)四种由一组固定mRNA目前正在评估和评估编码的肿瘤相关抗原组成cemiplimab (Libtayo; 赛诺菲/再生元)联用治疗 PD-1复发或难治性不可切除或转移性黑色素瘤。BioNTech(与基因泰克合作)有另一种基于mRNA恶性黑色素瘤候选疫苗BNT122(autogene cevumeran),新抗原和患者特异性疗法。Moderna默沙东还联合开发了一种新型抗原特异性mRNA个性化疫苗mRNA-4157,与帕博利珠单抗联合使用。
不可切除或转移性恶性黑色素瘤的过继性细胞疗法仍处于早期临床开发阶段。Lifileucel(Iovance Biotherapeutics)和ITIL-168(Instal Bio)是自体肿瘤浸润淋巴(TIL)细胞列细胞疗法II在期试验中进行研究。Lifileucel在两个试验中:接受过的PD-1治疗病人的实验(C-144-01)而且针对不接受PD-1治疗病人的实验,包括与帕博利珠单抗联用的评估(IOV-COM-202)。Lifileucel基于C-144-01获得了测试数据FDA认定再生医学先进疗法资格。ITIL-168在接受过PD-1单药疗法对治疗患者进行评价 (DELTA-1),并获得FDA孤儿药认证。
诺华正在开发目标PD-1和LAG-3联合疗法,即spartalizumab LAG525。其正处于II期试验PLATforM之前用于治疗的不可切除或转移性黑色素瘤。
Tebentafusp(Kimmtrak;Immunocore)是一种靶向gp100并与CD3抗体片段融合的双特异性可溶性高亲和力T细胞受体(TCR)治疗 。恶性黑色素瘤。Ib/II在期试验中,该药物与阿斯利康有关PD-L1抑制剂伐利尤单抗(Imfinzi)和/或CTLA-4用于西木单抗的抑制剂。Tebentafusp2022年1月成为第一个获得者FDA葡萄膜黑色素瘤的批准治疗TCR疗法。
市场指标
20212000年,恶性黑色素瘤疗法在主要市场的销售额为47亿美元,其中大部分(72%)由免疫检查点抑制剂持有:纳武利尤单抗(14亿美元)、帕博利珠单抗(13亿美元)和伊匹木单抗(7.31亿美元)。鉴于批准治疗的增加(包括标签扩展)和新药的批准,恶性黑色素瘤市场预计每年增长5%,到2030年将达到72亿美元(下图)。
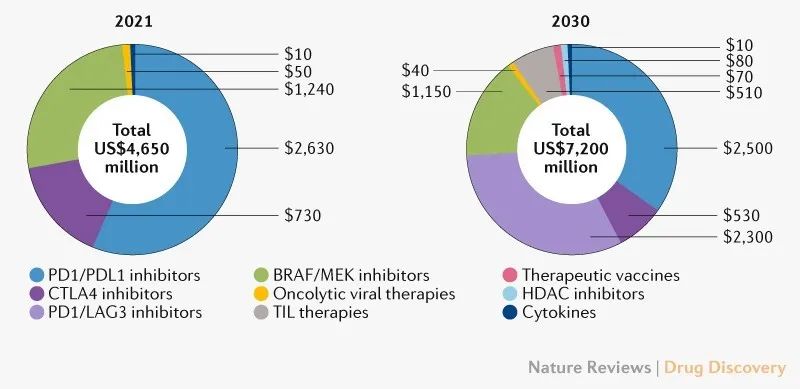
图1 | 皮肤恶性黑色素瘤关键疗法主要市场的估计销售额(按药物类别)。2021年(左)和2030年(右),美国、法国、德国、意大利、西班牙、英国和日本的销售额。
预计到2021年至2030年,检查点抑制剂将继续占据主导地位,到2030年将占据74%的市场份额。最近批准的抗性LAG-3/PD-1联合疗法Opdualag预计将成为最畅销的疗法(23亿美元),其次是帕博利珠单抗(13亿美元)和纳武利尤单抗(12亿美元)。尽管如此Opdualag无长期OS数据显示,与纳武利尤单抗 伊匹木单抗相比,其疗效可观(即PFS)和较小的副作用将促进该疗法的使用,从而促进销售。
2021年至2030年,恶性黑色素瘤市场联合疗法将逐步增多。预计到2030年,联合疗法将占据约58%($42亿)。BRAF/MEK抑制剂组合预计占总市场的15%;恩可非尼 比尼替尼将成为2030年商业上最成功的BRAF/MEK疗法(7.061亿美元)PD-1/PD-L1和BRAF/MEK由于抑制剂的高毒性、高成本和与其他组合疗法的竞争,预计很难获得市场份额。
2021到2030年,其他值得关注的入市玩家包括first-in-class的TIL疗法lifileucel,预计2030年将获得5.09收入亿美元。HDAC抑制剂HBI-8000以及基于肽的疫苗IO102-IO103预计市场影响较小,每种疫苗收益不足1亿美元,主要是早期联合治疗竞争引起的。

