ADC安全问题 从作用机制理解临床数据
文章来源:医药魔方Med
作者:阿拉蕾
抗体偶联药物(ADC)设计的初衷是通过靶向降低化疗药物引起的毒性。传统化疗药物,非结合型(unconjugated)细胞毒性药物在游离状态下分布在全身,这在很大程度上取决于它们的作用机制。至于细胞毒性药物,ADC抗体的特异性、连接器的稳定性、载荷的性质等因素使其具有不同于传统细胞毒性药物的毒性特征。
图片来自genentech官网
ADC相关毒性概述
根据现有报告,ADC相关毒性主要包括:血液系统毒性、神经毒性、肺毒性、皮肤毒性、肝毒性、眼毒性、代谢异常、心脏毒性、液体相关事件等。
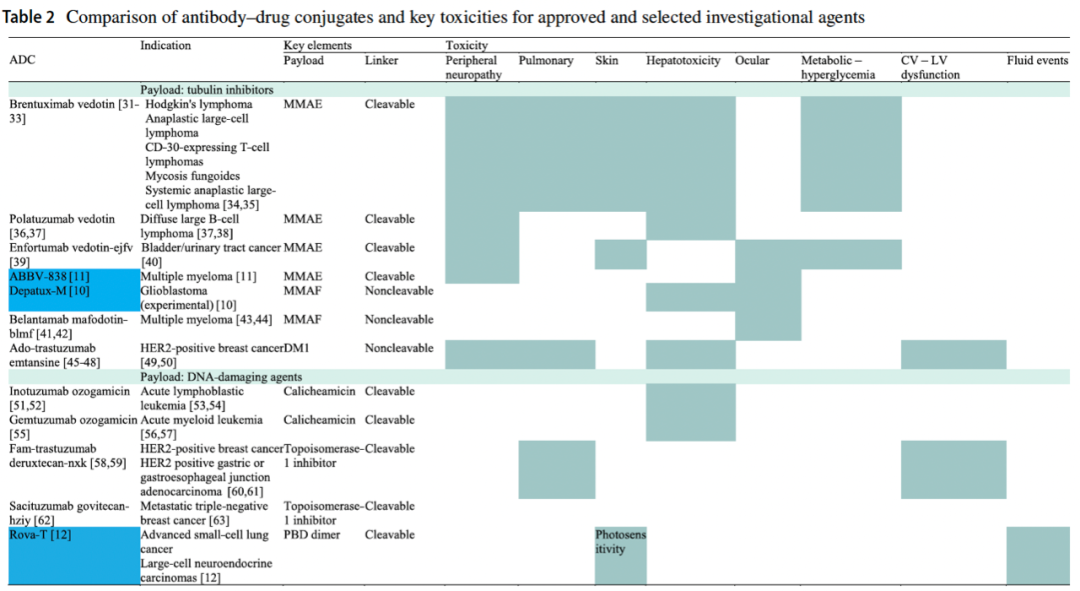
各ADC比较毒性特征. 图片来源:Drug Saf. 2021;733-742.
不同的ADC,毒性特征不同(见上图)。例如:维布妥昔单抗常出现血液系统毒性、外周神经病变等。T-DXd(DS-8201)肺毒性发生率较高。临床试验阶段发现。Rova-T(抗DLL3-ADC)与液体相关事件(如:心包积液、肢体水肿等)的发生有关。
影响ADC毒性的主要因素是什么?我们主要从与靶点有关的非肿瘤组织毒性开始(on-target,off-tumour)以及与脱靶有关的非肿瘤组织毒性(off-target,off-tumour)讨论两个方面。
on-target,off-tumour
靶向抗原的表达模式会影响细胞毒性药物的分布和聚集。靶向靶向药物。Lewis Y抗原的ADC BR96-以阿霉素为例,抗原也表达在人体的非肿瘤组织中,尤其是胃肠道。与传统的阿霉素给药方法相比,BR96-阿霉素不会引起明显的血液学或心脏毒性,但近90%的患者有≥2阿霉素传统给药方法的发病率为22%),还观察到淀粉酶和/或脂肪酶的升高和呕血,这在阿霉素传统给药时没有观察到。
另一个例子是使用靶向CD44的ADC bivatuzumab mertansine,近80%的患者有皮肤毒性,包括中毒性表皮坏死松解症,导致部分患者表皮严重或致命脱落。目前认为与皮肤上靶蛋白的表达有关。
另外,虽然有相同的载荷(都是)MMAE)、所有可切割连接器均采用(linker)、药物-抗体比例(DAR)相近(3.5~4),但维布妥昔单抗(靶点是维布妥昔单抗)CD30)、polatuzumab vedotin(靶点为CD79b)和 enfortumab vedotin(靶点为nectin-4)毒性特征也有差异。例如,40%使用。enfortumab vedotin患者有味觉障碍,可能与唾液腺有关nectin-4表达方式有关brentuximab vedotin或polatuzumab vedotin这种毒性在关键临床试验中没有观察到。
再举一个例子,具有不同载荷的新型抗性HER2-ADC:T-DXd(DS-8201)和trastuzumab duocarmazine肺毒性发生率高,具体机制尚不清楚。有趣的是,抗性是,抗性是有趣的。HER2-ADC T-DM1心脏毒性似乎低于曲妥珠单抗。原本预计。ADC可能会导致更高的心脏毒性,因为ADC直接向表达HER2心肌细胞释放负荷,但临床上尚未观察到这种预测,造成这些差异的原因尚不清楚。
off-target,off-tumour
与靶向相关性毒性相比,脱靶相关性的不良反应可能是ADC毒性的主要因素。现有数据显示,不考虑抗体部分、载荷、载荷。MMAE与贫血、中性粒细胞减少、周围神经病变有关;DM1与血小板减少、肝脏毒性有关;MMAF和DM4与眼毒性有关。这种脱靶毒性可能主要与循环、非肿瘤组织、肿瘤微环境等负荷有关(TME)与相关非肿瘤组织的后续影响有关。
而且,这种脱靶毒性可能与负荷类型关系不大。例如,无论如何,无论如何,无论如何。ADC目标是什么,MMAF眼毒性常见,而且MMAE发病率不高,虽然这两种药物都属于auristatin类细胞毒性药物(微管蛋白抑制剂)。
与可切割连接器相比,不可切割连接器在血浆中更稳定,但其抗体抗体更稳定-连接子结构依靠溶酶体降解来释放载荷,这往往导致载荷上的带电氨基酸保留,这可能会影响药物的疗效或细胞的渗透性。
MMAF通常由不可切割的连接器递送,从连接器上释放后,MMAF在角膜上皮细胞中积累电荷是可能的。MMAE通常通过可切割的连接器,疏水性更强,能穿透细胞膜磷脂双层,因此可扩散角膜上皮细胞。
然而,无论连接器的类型如何,几乎都是这样DM4为载荷的ADC,还有一部分DM1为载荷的ADC观察到眼毒,表明这种毒性并不完全归因于带电负荷。
值得注意的是,一些已知靶抗原在眼睛中表达ADC,没有显示出眼毒性。对于某些部位。ADC目标抗原可以在非肿瘤组织中表达,但其水平不足以引起毒性。TROP2以戈沙妥珠单抗的靶抗原为例TROP2在动物模型试验中,戈沙妥珠单抗(sacituzumab govitecan)单独使用的毒性特征和载荷的毒性特征SN-38相当,这也提示了在ADC在毒性方面,脱靶毒性可能是主要因素。
ADC毒性问题非常复杂,下图综合显示ADC潜在的非肿瘤细胞毒性机制,除了靶抗原表达外,不依赖靶抗原ADC摄入也是一个重要因素,包括:1、能与能与能,ADC IgG抗体Fc段组合的受体,如Fcγ受体(FcγR)、新生儿Fc受体(FcRn)、C型凝集素受体(CLR)。2、非特异性内吞机制(如巨胞饮和微胞饮)可以内化整个内吞机制ADC或游离载荷;3.由于连接子不稳定或细胞外蛋白酶,载荷在细胞外释放。5.旁观者效应。
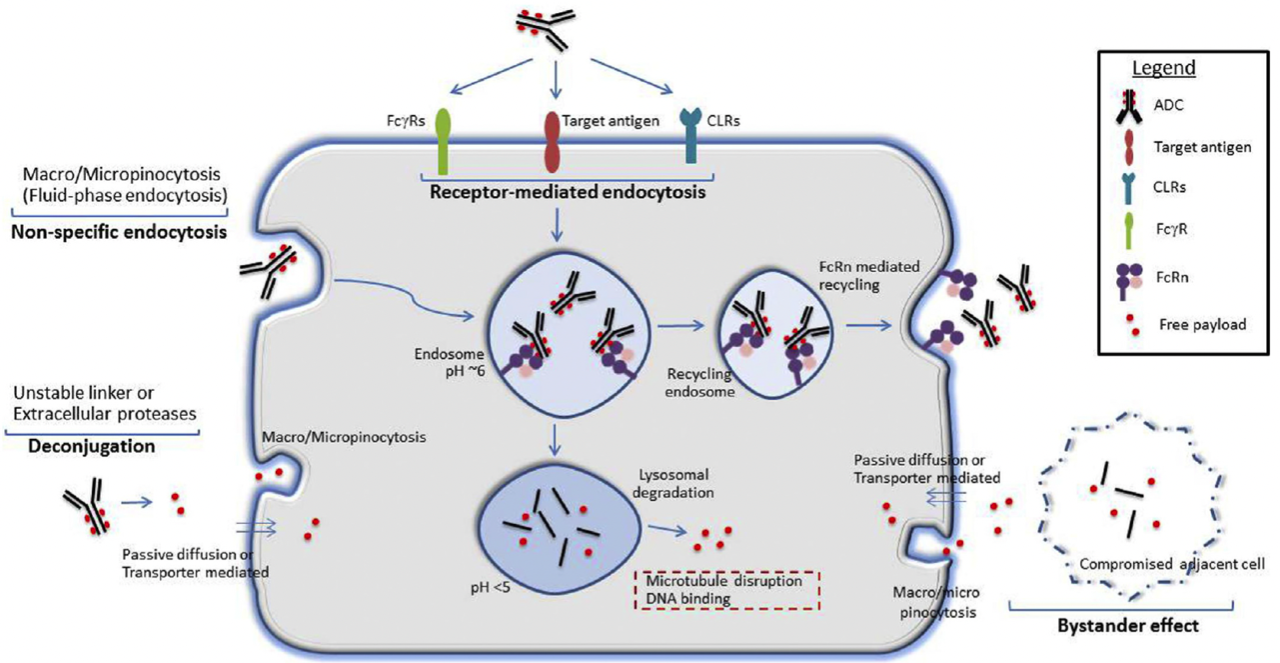
举个例子,T-DM1相关的血小板减少症可能部分是由于未成熟的巨核细胞通过FcγR摄取ADC,这影响了巨核细胞的正常分化。临床前研究数据显示,部分临床前研究数据显示,部分临床前研究数据显示,ADC靶抗原不在眼睛里表达,细胞饮酒是引起眼毒性的可能原因。
另外,同一个ADC不同类型的肿瘤也会表现出不同的毒性特征。在相同剂量下,glembatumumab vedotin(靶点是gpNMB)可导致30%的黑色素瘤患者出现严重皮疹(包括1例死亡病例),但乳腺癌患者中只有4%。在不同类型的肿瘤中,肿瘤相关抗原对免疫系统的激活特征可能不同,但这种现象的具体原因尚不清楚。
最后:现有数据提示我们,仅根据现有数据,ADC结构难以完全预测ADC在进行临床试验或实际临床应用时,应注意监测、剂量选择和不良事件报告的重要性。同时,我们也期待着临床前和基础转化研究的进一步深化。

