默克c-Met抑制剂在华上市 国内多企布局 后来者还有机会吗?
小时光
330月30日,中国国家食品药品监督管理局药品评价中心(CDE)官方网站公布,德国默克(Merck KGaA) 接受盐酸特泊替尼上市申请。
图1. 盐酸特泊替尼上市申请受理:CDE官网
特泊替尼(tepotinib,商品名Tepmetko)是一款口服c-MET抑制剂已在日本和美国获批上市,用于治疗携带MET外显子14(MET ex14)非小细胞肺癌(NSCLC)患者。
1
c-MET与癌症
间质表皮转化因子 (c-Mesenchymal-epithelial transition factor,c-Met)它是一种由受体酪氨酸激酶编码而成的蛋白质c-Met能与肝细胞生长因子(HGF)一种受体酪氨酸激酶。
c-MET促进组织分化和修复,调节异常时促进肿瘤细胞的增殖和转移。MET通道异常激活发生在许多实体肿瘤中,包括脑癌、乳腺癌、结直肠癌、胃癌、头颈癌、肺癌、肝癌、皮肤癌、前列腺癌和软组织癌等。这种异常激活可以通过非HGF依赖机制的发生主要包括MET 14号外显子跳跃突变MET扩增、重排和MET蛋白质表达过多。
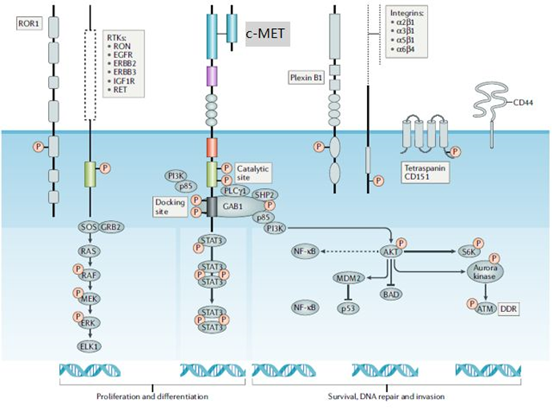
图1. c-Met相关信号通路示意(参考2)
c-MET已成为癌症领域的热门研究目标之一。目前,小分子学已成为目前癌症领域的热门研究目标之一。c-Met抑制剂又分为单靶点或多靶点c-Met抑制剂。
单靶点c-Met抑制剂可以锚定Met更独特的铰链区域,高选择性抑制Met激酶;
而多靶点c-Met抑制剂可以靶向多种激酶VEGFR活性远高于Met活性,用于靶向Met致癌突变比较勉强,比如Crizotinib(克唑替尼)等。
因此,我们主要了解单靶点c-Met抑制剂。
2
c-Met抑制剂代表药物
世界上第一个获批的c-Met抑制剂-特泊替尼
特泊替尼是世界上第一个获批的特泊替尼c-Met抑制剂,最早于2020年3月25日获得日本厚生劳动省批准,并在日本上市。2020年8月26日,FDA特泊替尼治疗优先考试资格MET ex14突变的转移性NSCLC病人。在此之前,特泊替尼曾被称为特泊替尼。FDA被授予突破性疗法称号,并被日本厚生劳动省授予创新药物资格和孤儿药称号,可以说是备受好评。
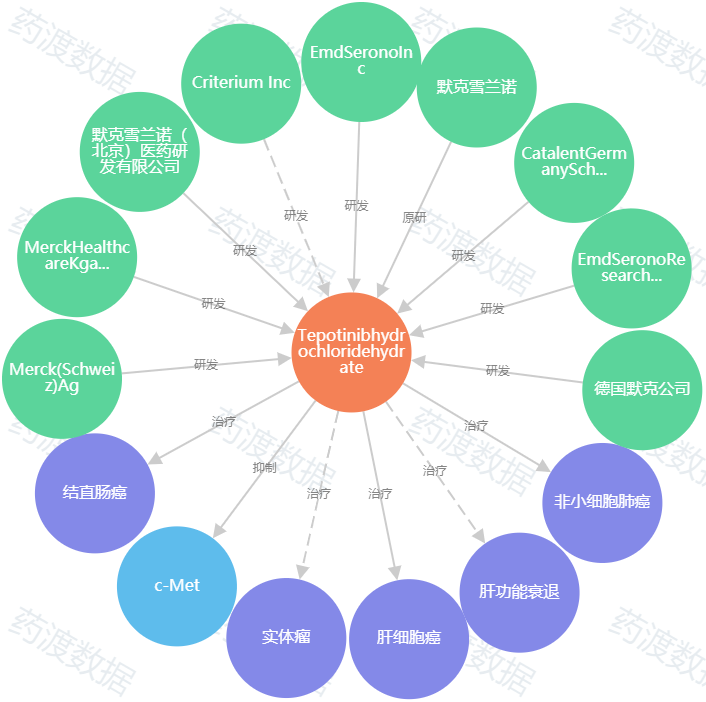
图2. 特泊替尼知识地图来源:药渡数据
特泊替尼在日本和美国获批的关键临床试验是一项名为特泊替尼的关键临床试验VISION单臂、多中心、开放标签临床II期间研究。共携带152人。MET ex14突变的晚期或转移NSCLC患者接受特泊替尼单药治疗。他们不携带。EGFR或ALK基因突变。
结果表明,特泊替尼在初治和经治患者中总缓解率为43%。初治和经治患者中位缓解持续时间(DOR)分别为10.8个月(95% CI,6.9-NE)和11.1个月(95% CI,9.5-18.5)。676个月以上,30%的初治患者和50%的经治患者持续6个月以上。
首款获FDA批准的c-Met抑制剂卡马替尼
卡马替尼(Capmatinib,商品名Tabrecta)是首款获FDA批准的c-Met抑制剂。诺华公司(Novartis)2020年5月6日研发,FDA批准卡马替尼上市治疗MET ex14突变的NSCLC患者。
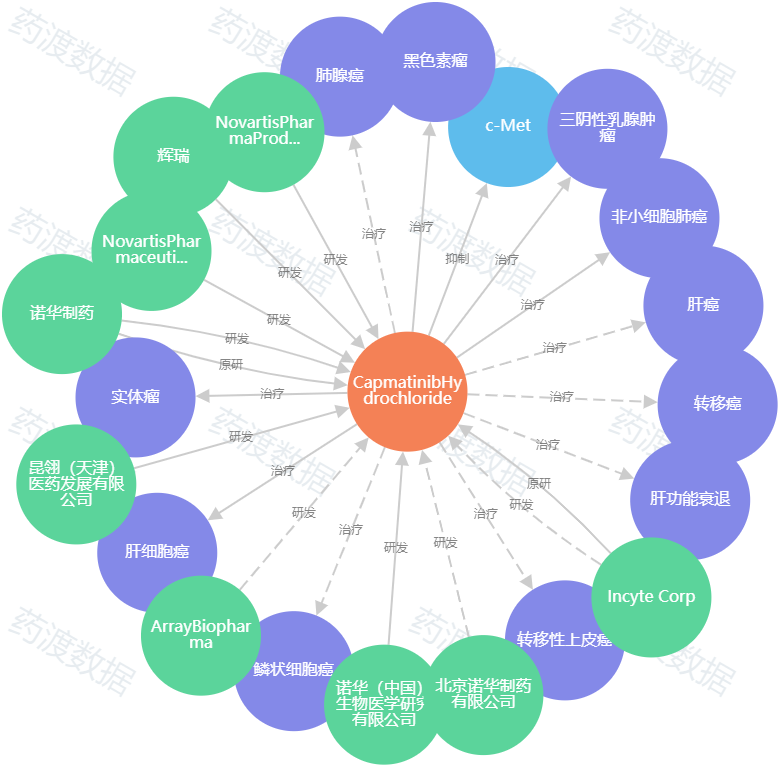
图3. 卡马替尼知识地图来源:药渡数据
该批准是基于卡马替尼的Ⅱ期GEOMETRY mono-1该试验是多中心、非随机、多队列的试验Ⅱ期临床试验,入组97例,MET ex14突变的晚期或转移NSCLC病人。主要评价指标是客观缓解率(ORR)及DOR。
研究结果表明,在28例初治患者中,ORR68%(其中4%为完全缓解,64%为部分缓解),DOR为 12.6个月;69例经治病人中,ORR为41%为41%(41%),DOR为 9.7个月。
国内首款获批c-Met抑制剂-赛沃替尼
赛沃替尼(Savolitinib,商品名Volitinib)由和黄医药研发,于2021年6月22日获得NMPA批准上市治疗MET ex14局部晚期或转移性突变NSCLC病人。这是中国第一个申请上市的人。c-Met抑制剂,也是赛沃替尼全球首个新药上市申请。
图4. 赛沃替尼知识地图来源:药渡数据
其批准是基于开放,II该研究包括中国32个中心的70个MET ex14突变NSCLC病人,中位随访17.6结果显示,在疗效可评估的61名患者中,ORR为49.2%,疾病控制率(DCR)为93.4%,产生应答的中位时间为1.4个月,DOR为8.3一个月。此外,和黄医药也在开发赛沃替尼的胃癌和结直肠癌适应症,都到了。II期阶段。
3
国内小分子c-Met抑制剂研发现状
谷美替尼海和药物
谷美替尼是由上海和中国科学院上海药物研究所合作开发的小分子c-Met抑制剂。临床研究表明,谷美替尼强效和特异性靶向抑制MET激酶活性。初步临床研究结果表明,谷美替尼具有优异的药代动力学特性、良好的安全性和耐受性,药物半衰期长,稳态谷浓度高,有利于靶点的持续抑制。谷美替尼正在MET ex14突变的NSCLC初步疗效显示。
图5. 谷美替尼知识地图来源:药渡数据
20219月,谷美替尼被CDE纳入突破性治疗品种;2022年1月,谷美替尼还获得了美国FDA授予的孤儿药资格用于治疗MET基因变异的NSCLC患者。
伯瑞替尼
伯瑞替尼由北京浦润奥生物科技公司自主研发。2020年,伯瑞替尼治疗c-Met异常的晚期NSCLC的I临床试验结果出现AACR年会。
图6. 伯瑞替尼知识地图来源:药渡数据
该研究在37名经治但未被接受c-Met抑制剂或HGF靶向治疗、局部晚期或转移晚期NSCLC结果显示,在所有36名可评估疗效的患者中,伯瑞替尼ORR为30.6%,DCR为94.4%。在亚组分析中,在携带中,c-Met过度表达、扩增或ex14在跳跃突变患者中,ORR分别为30.6%、41.2%和66.7%。
目前,伯瑞替尼被CDE计划纳入突破性治疗品种,治疗MET ex14突变的NSCLC病人。此外,该药物还计划用于治疗神经胶质瘤、肾细胞癌(RCC)和肝细胞癌(HCC)。
此外,国内还有江苏豪森HS-10241临床试验正在进行中,适应证为MET ex14突变的NSCLC,此外,肝癌和胃癌的适应证也在临床研究中。
4
小分子c-Met抑制剂市场前景
3%的非小细胞肺癌-5%的病人会出现MET基因扩增或外显子14突变,预后差,对传统化疗和免疫治疗不敏感。我国每年新发肺癌80多万例,其中非小细胞肺癌约占80%-85%,在这个庞大的患者基数下,3%-5%的突变频率也对应于少数患者,这些患者急需低毒高效的靶向新药上市。
另外在接受EGFR-TKI在治疗耐药性患者中,约50%是T790M另有约20%的患者是突变患者c-Met扩增。对这些病人来说,c-Met抑制剂成了良药。
目前国内布局小分子c-Met抑制剂公司大多处于研发初期,由于抑制剂公司大多处于研发初期,MET基因变异与多种癌症有关,有利于适应证的差异化布局,避免同质化竞争。
总之,留在中国c-Met抑制剂市场充足。然而,因为,因为,因为,因为,因为。c-Met它已成为研究人员开发癌症(特别是非小细胞肺癌)靶向药物的热门靶点之一。除了单靶点抑制剂外,它还针对单靶点抑制剂c-Met多靶点抑制剂、双抗和抗体偶联药物(ADC)等等,国内有十余款c-Met靶向药物已进入临床阶段,因此要想抓住市场机遇,只有快不破。
参考资料:
1.CDE官网
2.Puccini,A.,et al. (2019). Safety and Tolerability of c-MET Inhibitors in Cancer. DrugSafety. doi:10.1007/s40264-018-0780-x;
3.Comoglio PM,Trusolino L,Boccaccio C.Known and novel roles of the MET oncogene in cancer: a coherent approach totargeted therapy. doi: 10.1038/s41568-018-0002-y.
4.药渡数据库 https://data.pharmacodia.com
