第三波新药研发-小核酸药物(1)
发布时间: 2022-03-11 10:42:25
基因疗法是当今最前沿的技术之一,在治疗肿瘤、遗传性疾病、代谢性疾病、预防性传染病等方面取得了突破。其中,小核酸药物是发展最快的基因疗法之一,正成为第三波新药研发的领导者。
小核酸药物简介
小核酸药物主要包括反义寡核苷酸(ASO)、小干扰RNA (siRNA)、微小RNA (miRNA)、小激活RNA (saRNA)、信使RNA (mRNA)、RNA适配 (Aptamer)等。
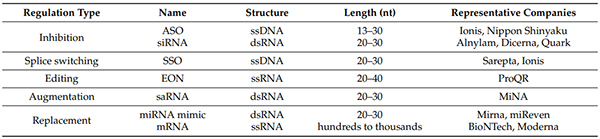
核酸药物分类[1]
反义寡核苷酸 (ASO)技术原理:技术原理:ASO 分子量小(约 )18-30 核苷酸)是一种合成的单链核酸聚合物,可通过多种机制调节基因表达。ASO 调节基因表达的方式有三种:第一种:ASO 与 mRNA 结合后,形成空间位阻,使 mRNA 不能再进入核糖体进行蛋白质翻译,使这种 mRNA 所携带的基因信息表达下降。ASO 通过碱基互补配对,与靶标 mRNA 结合后,招聘 RNA 酶将 mRNA 降解也降低了基因表达。第三:主要针对 pre-mRNA 在形成 mRNA在 的过程中,ASO 结合于 Pre-mRNA 的一个外显子区域使这个外显子在最终生成的 中被切断mRNA 不包含这种外显子。
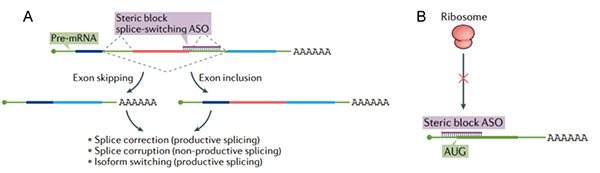
ASO[2]
RNA干扰 (RNA interfering; RNAi)技术原理:反义 RNA 与靶基因的 mRNA 以碱基互补配对的形式结合,导致序列特异性基因沉默。长链双 RNA (dsRNA) 被剪切为siRNA (小干扰 RNA) 后,与蛋白质结合形成 siRNA 诱导干扰复合体 (RISC),RISC再加上互补 mRNA (信使 RNA) 结合,使靶基因 mRNA 降解,最终沉默特定基因表达,实现基因治疗,调节患者体内特定靶基因表达。
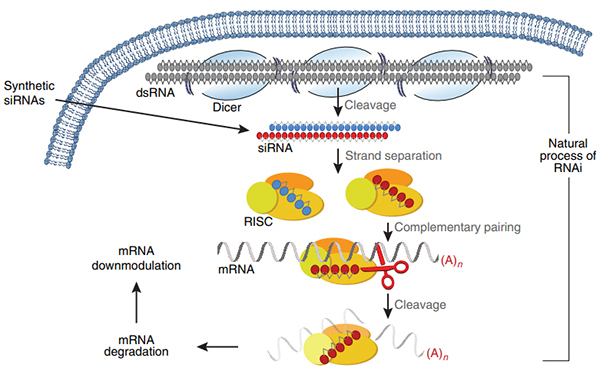
RNAi[3]
小核酸药物发展史
- 1978 年,哈佛大学科学家Paul Zamecnik 等人首次报道了反义寡核苷酸 (antisense oligodeoxynucleotides) 可抑制肉瘤病毒的复制;
- 1998 年,全球首款 ASO 药物 (反义寡核苷酸药物) Vitravene批准上市;
- 1998 年,Andrew Fire 和 Craig Mello 在线虫中首次曝光RNAi凭借这一发现,2006年获得诺贝尔生理学与医学奖;
- 2001 年,RNAi 技术被 Science 杂志评为 2001 年十大科学进展之一;
- 2004 年,OPKO 公司首次用于老年性黄斑变病 siRNA 药物 Bevasiranib 进入临床试验;
- 2005-2016 年,由于小核酸技术领域的技术瓶颈没有突破,药物本身的特点和商业化过程中的各种问题导致该领域进入低谷;
- 2016 年,SareptaTherapeutics 和 Ionis 开发的 2 型ASO 药物先后被 FDA 批准上市;
- 2018 年,全球首款 siRNA 药物即 Alnylam 公司的 Onpattro 由 FDA 批准上市,用于 hATTR 治疗多发性神经病患者;
目前,全球有超过 20 余款 siRNA药物,50 余款 ASO 药物正处于临床研究阶段,涵盖中枢神经系统、心血管系统、抗感染和抗肿瘤。
全球小核酸药物发展现状
国外小核酸药物研发概况:目前全球上市的小核酸药物共有 15 款,约85% 2015年以后上市。Ionis、Alnylam、Sarepta 是小核酸药物领域的三巨头。
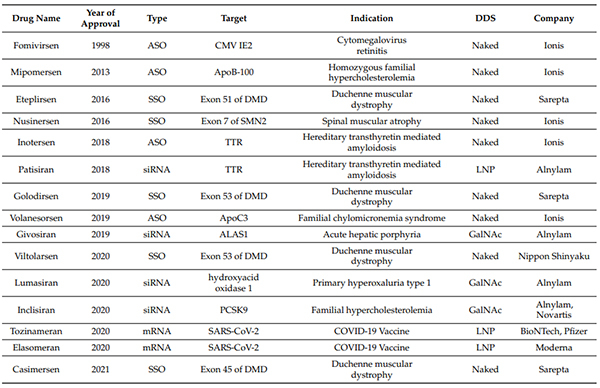
FDA/EMA经批准的核酸药物 (截至2021年6月30日)[1]
国内小核酸药物研发概况:与国外相比,国内小核酸药物尚未获批,国内小核酸药物企业仍处于发展初期或上升期。国内中小型核酸药物龙头企业包括苏州瑞博生物、苏州圣诺制药、中美瑞康等。

小核酸药物的特点及优点
- 特异性强:小核酸药物以目标为基础RNA人工设计,目标明确,靶点特异性强。
- 设计简单,研发周期短:小核酸药物临床研发首先通过测定基因序列,合理设计疾病基因,使基因目标沉默,避免盲目开发,大大节省研发时间。
- 靶点丰富:转录后小核酸药物可以突破一些蛋白质靶点有效的特殊靶点,有望克服没有药物的遗传疾病。
挑战和战略
小核酸药物开发过程中最大的问题是避免快速降解,进入靶向细胞,发挥治疗功能。目前,国内外技术相当成熟。随着基因测序技术的发展,测序成本降低,为小核酸药物的产业化提供了可能。小核酸药物开发过程中最大的困难是如何在注射小核酸药物后时间,准确进入靶向细胞,最大限度地避免正常细胞的意外伤害。
[4]
小核酸原料药生产采用固相合成技术,工艺开发、工艺放大和质量控制壁垒较高,小核酸原料药固相合成配套设备、清洁环境等早期投资非常大,生产需要满足 GMP要求。因此,国内能够生产小核酸原料药的企业很少,相关行业的配套设施也不完善。随着市场需求的增加,能否保证小核酸药物的及时供应已成为产品开发和商业化成功的重要挑战。
小核酸药物在体内不稳定,进入血液后容易被核酸酶降解,容易通过肾脏去除,半衰期短。同时,外源性核酸分子具有免疫原性,容易引起人体免疫反应。此外,如果不能进入细胞进行细胞吞咽,小核酸药物将无法发挥作用。这些问题可以通过化学修饰和传递系统来解决。随着技术的突破,一些问题得到了很好的解决,包括化学修饰 (如磷酸骨架、核糖、核糖五元环改造、碱基、核苷酸训练末端改造等)。) 可以避免核酸酶降解核酸药物,延长半衰期,高效安全的传递系统 (如环糊精纳米聚合物、脂质纳米颗粒、缀合物传递系统、乙酰半乳糖胺系统等。) 可以使核酸药物准确靶向目标细胞,提高细胞摄入效率,使核酸药物发挥治疗作用。
小核酸药物从转录后的水平进行治疗,可以突破难以成药的特殊蛋白质靶点,有望克服遗传性疾病等难治性疾病。
小核酸药未来发展趋势
未来,随着小核酸药物应用领域和技术领域的不断突破和创新,技术更新将有助于小核酸药物的发展。市场需求和市场规模将继续扩大,小核酸药物适应症范围广泛,包括肿瘤、罕见病、病毒性疾病、肾病、心血管疾病、炎症性疾病、代谢性疾病等。因此,小核酸药物的潜在适应性基础很大。随着技术的发展和生产的成熟,小核酸药物市场未来将有更广阔的发展空间。
与现有的小分子和抗体药物相比,小核酸药物具有目标筛选快、研发成功率高、耐药性差、治疗领域更广、效率更长等优点,具有很大的发展潜力。随着技术的不断进步,小核酸药物有望形成继小分子药物和抗体之后的第三波现代新药。
