罗氏Aβ抗体crenezumab再次临床失败AD研发将何去何从?
罗氏和班纳老年痴呆症研究所于2022年6月16日联合宣布,crenezumab早发性阿尔茨海默病没有减缓或预防(AD)特定基因突变的人的认知能力下降;虽然在共同的主要终点和多个次要终点和探索性终点中观察到它有助于 crenezumab 小数值差异,但这些差异没有统计意义。这是在2019年1月,罗氏终止crenezumab 治疗早期阿尔茨海默病患者的两项III期CREAD I和CREAD 2临床研究再次失败,使淀粉样蛋白失败(Aβ)药物研发再次遭遇重创。

API ADAD 最初的试验来自班纳阿尔茨海默病研究所(BAI) 研究人员提出,认知障碍尚未出现,但表现为AD一个前瞻性的、随机的、双盲的、安慰剂对照的平行组,在最早有生物迹象的患者中II 疗效验证研究。共招募了252名受试者,随机分配接受者crenezumab或安慰剂治疗,持续5-8年,其中94%的参与者完成了研究。结果表明,该实验在认知能力或情境记忆功能变化的两个共同终点上没有显示具有统计意义的临床效益;在研究过程中没有发现新的安全问题。进一步的数据将于2022年8月2日在阿尔茨海默病协会国际会议上发布(AAIC)上公布。
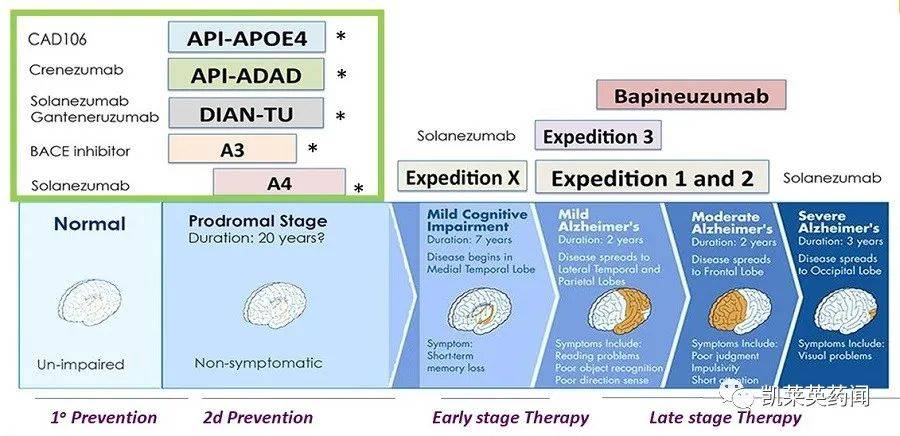
Crenezumab这是一个靶向Aβ作为罗氏的明星药物,数十亿美元和几十年的努力一度化为乌有。随着人口老龄化的加深,AD以神经退行性疾病为代表的神经退行性疾病已成为现代社会严重的医学问题;然而,由于这些疾病的发病机制复杂,目前尚不清楚。在神经退行性疾病的治疗过程中,血脑屏障是一个很大的瓶颈(BBB)它的存在影响了药物在大脑中的有效传递,使得许多药物很难进入大脑发挥功效。作为新药研发的重灾区,AD临床试验失败率高达99.6%。
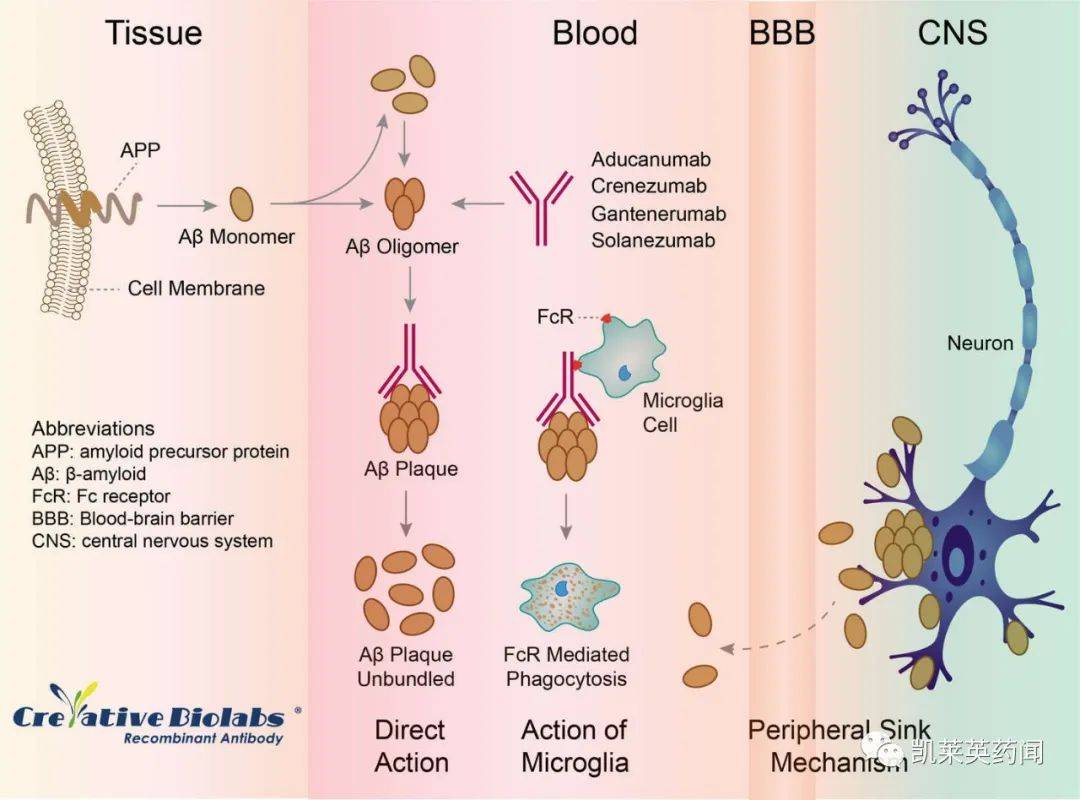
2022年3月,发表了一篇文章Nature Reviews Drug Discovery在文章中,治疗AD的Aβ假设提出了新的见解。Aβ假说认为,因为Aβ42或其它Aβ多肽片段产生过多或未及时清除,导致可溶性Aβ大脑中沉积的寡聚体和不溶性淀粉样蛋白形成淀粉样蛋白斑块。然而,根据已经进行的研究,tau神经纤维缠结由蛋白质组成(NFT)的扩展与AD患者认知障碍具有较好的相关性,Aβ沉积与认知障碍之间没有直接和显著的相关性;只有大脑中的可溶性Aβ和/或淀粉样蛋白斑块的水平降低到非致病性水平,即不能促进tau蛋白质病理学水平的扩展——Aβ的PET指标降至20CL只有这样,才有机会获得临床效益。解决这些问题的方法之一是开发更敏感的新临床指标,使其能够AD在早期阶段,观察到患者认知水平的微妙变化。另一种解决方案是进行预防性治疗的临床试验,罗氏的临床试验API ADAD 试验就是这类试验。
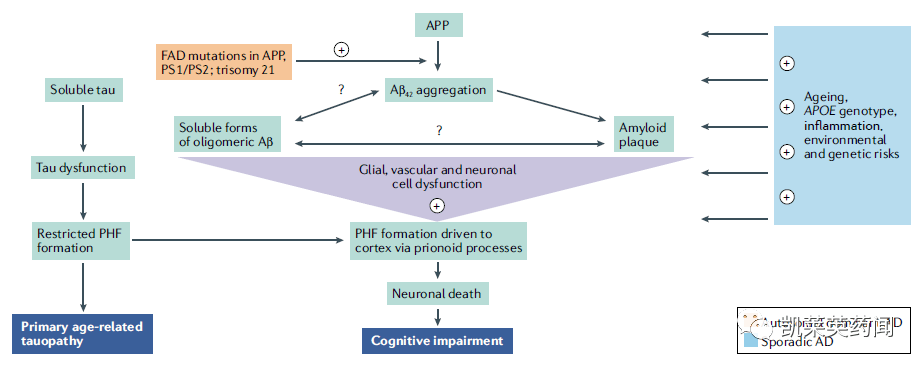
纵观针对Aβ目前,抗体的开发只得到了卫生材料和渤海共同开发aducanumab,年销量170万美元,2021年。AD千亿市场,aducanumab处方的热情明显不足。药物批准只是第一步。临床医生和患者是否能被说服是药物最终成功的关键。此外,卫生材料/渤海建筑共同开发lecanemab、礼来的donanemab、罗氏的gantenerumab还得到了美国FDA认定突破性疗法。lecanemab是继aducanumab之后,卫材和渤健针对AD二次合作,如法炮制lecanemab能否安全上市,得到社会各界的认可,还有待进一步发展。在此之前,礼来是在New England Journal of Medicine公布donanemab针对早期AD患者的II期测试数据好坏参半,在一种疾病的量表上取得了微弱的胜利,但在更广泛使用的阿尔茨海默病量表上失败了。同样,罗氏的目标是gantenerumab展开了GRADUATE-1和GRADUATE-这项研究预计将于2022年第四季度公布。除此之外,国内企业恒瑞和先声药业也是对的Aβ抗体一抛千金,针对Aβ抗体的发展是九死一生还是昙花一现,未来最终会给出答案。
目前在研的Aβ抗体
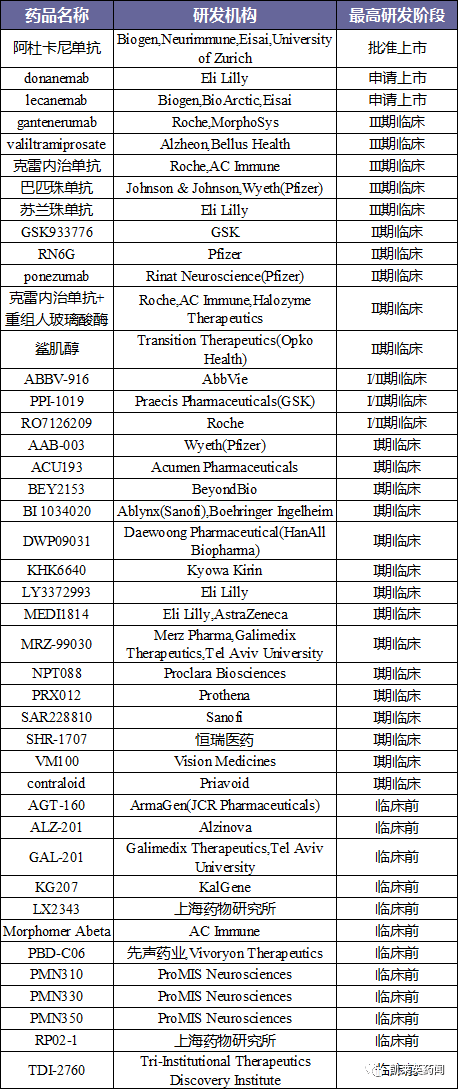
据报道,目前世界上至少有5000万人AD到2050年,患者预计将达到1.5亿左右。中国是世界上的一个患者AD在中国65岁以上的人口中,人数最多的国家,AD患病比例为3.21%。未来,随着我国社会老龄化问题的日益突出,预计到2050年患者人数将达到4000万左右。面对重大未满足的临床需求,我们期待更多的研究和新的临床诊断指标,以促进该领域药物的批准。
