诺华LNP国家食品药品监督管理局受理023胶囊上市申请
发布时间: 2022-03-03 13:36:59
3月3日,国家药品监督管理局药品评价中心(CDE)最新公示,诺华(Novartis)LNP接受023胶囊上市申请。
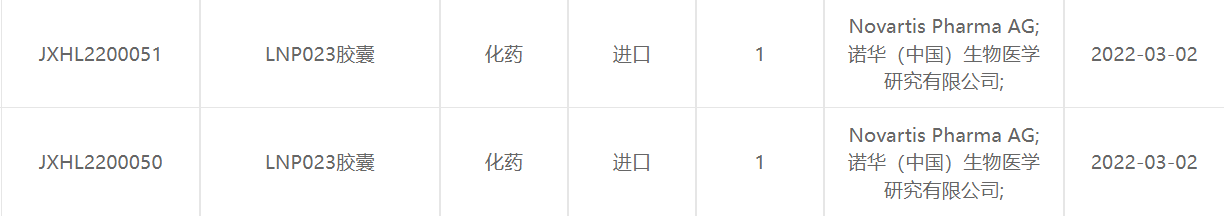
截图来源:CDE官网
LNP023是诺华开发的口服,具有特殊性first-in-class”补体因子B抑制剂可以用靶向补体代替信号通路,阻断血管和血管之间的溶血。目前,这种创新疗法用于治疗阵发性睡眠性血红蛋白尿症(PNH)、特发性膜性肾病、IgA肾病,原发性IgA以及本次获批的肾病,以及本次获批的肾病,C3肾小球病。
该药于2020年5月获批临床实践,开发适应症为特发性膜性肾病(IMN)。IMN它是临床上常见的肾病,也是成人肾病综合征最常见的病理类型,膜性肾病75%~80%是特发性的。近年来,其发病率有所上升,尤其是年轻病人。在此之前,LNP023还获得针对IgA肾病临床试验默示许可。
