接受通化东宝利拉鲁肽注射液上市许可注册申请
发布时间: 2022-06-08 19:44:26
6月8日,通化东宝发布公告,近日收到国家美国食品药品监督管理局关于利拉鲁肽注射液上市许可证注册申请的受理通知书,受理号为:CXSS2200058国。

利拉鲁肽是一种人类胰高血糖素样肽-1(GLP-1)类似物,可激活人类GLP-促进胰腺分泌胰岛素的受体。该品种由诺和诺德公司生产(NOVO NORDISK)开发于2011年进入中国市场,被批准用于成人2型糖尿病患者血糖控制。此外,利拉鲁肽还具有显著的减肥效果,减肥适应症产品(Saxenda)2014年12月在美国上市。
2018年9月,公司获得国家药品监督管理局批准发布的《利拉鲁肽原料药审批通知书》和《利拉鲁肽注射液临床试验批准书》,批准文件编号分别为2018L03096、2018L03097;2020年7月获得Ⅰ2021年10月获得临床试验总结报告Ⅲ期临床试验总结报告;2022年6月8日,国家药品监督管理局受理了该公司利拉鲁肽注射液上市许可证注册申请。
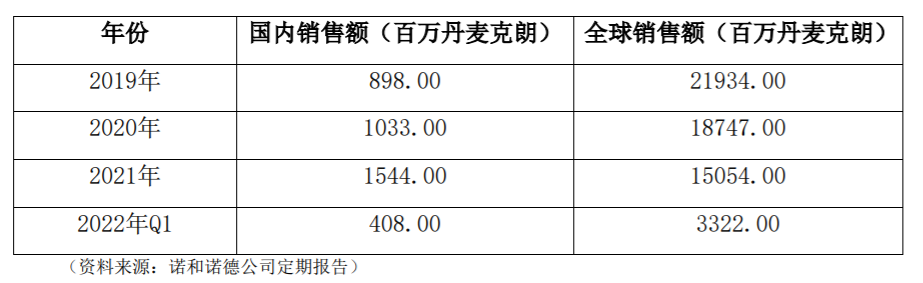
根据国际糖尿病联盟(IDF)全球糖尿病地图(第10版)显示,2021年20-79岁的成年人中有5名.37亿糖尿病患者,相当于每10个人中就有一个糖尿病患者。目前,中国仍然是糖尿病患者数量最多的国家,2021年20-79岁的成年糖尿病患者已经达到10.4亿人。近年来,GLP-1.受体激动剂在糖尿病治疗中的地位正在上升,市场正在迅速扩大。诺和诺德的利拉鲁肽注射液(Victoza)销售数据见下表。