B7-H3篝火的靶点再次升起 天生生物、百奥泰、博生吉领潮
文 | 笃行
415月15日,百奥泰宣布BAT8009获批临床,BAT8009是一款靶向B7-H3的ADC药物。3月9日,百奥泰发布公告,其下另一款ADC药物——BAT8006获批临床,BAT8006是一款靶向FRα的ADC药物。
FRα和B7-H3 ADC药物的再启航标志着百奥泰的再战ADC赛道。当然,,赛道。B7-H3和FRα作为一个新的目标,也意味着可参考的数据相对有限,风险与收益并存。
01
B7-H3靶点简介
T细胞活化取决于两个信号,包括第一信号和第二信号。第一个信号是指抗原呈现细胞。(APC)上的抗原肽-MHC分子复合物和T细胞受体TCR特异性识别,即T细胞对抗原的识别;第二个信号是指细胞对抗原的识别;T细胞与抗原呈现细胞表面的许多协同刺激信号,即共同刺激分子(Costimulation)。
一般认为,B7与细胞(主要是T细胞)的受体组合作为第二个信号发挥作用。例如,抗原呈现细胞。(APC)表面的B7-1或B7-2与T细胞表面的CD28结合,促进T细胞增殖、分泌、提高抗凋亡基因;与抗凋亡基因;CTLA-4结合,则抑制T进一步激活细胞,有利于肿瘤细胞的逃逸。尽管如此。B7-1可以与CD28和CTLA-4结合,但与CTLA-4亲和力的结合是CD28的20倍以上。
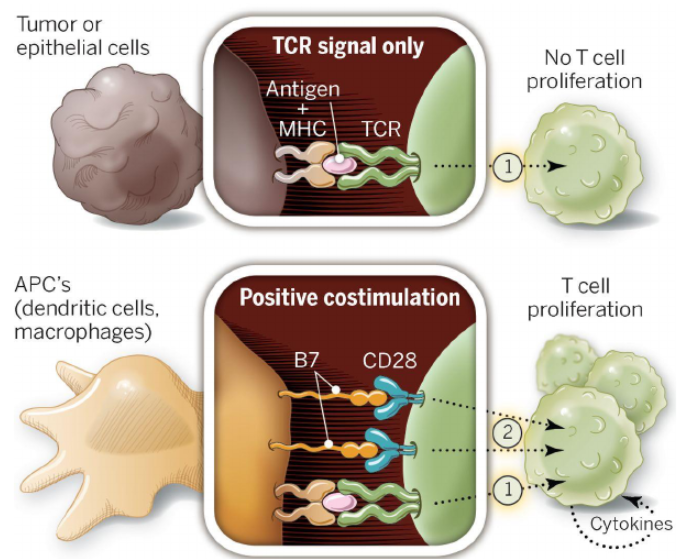
图:T细胞活化通道
数据来源:Cancer Discovery
B7家庭成员广泛表达在非淋巴组织中,不同的B7分子在调节免疫细胞反应时产生不同的正负共刺激信号。目前已发现10多种。B7蛋白质分子,包括更多的研究B7-1(CD80)、B7-2(CD86)、B7-H1(PD-L1)、B7-H2(ICOSL)等等。正是因为部分B7蛋白质的作用,使T抑制细胞功能,导致肿瘤免疫逃逸。因此,通过阻断,通过阻断。B7结合其配体,有望提高肿瘤治疗的疗效。如近年来的大红大紫。PD-(L)1抑制剂与CTLA-4抑制剂在临床实践中得到了准确的验证,在各种肿瘤中表现出良好的治疗效果。
表:常见的B7家族成员
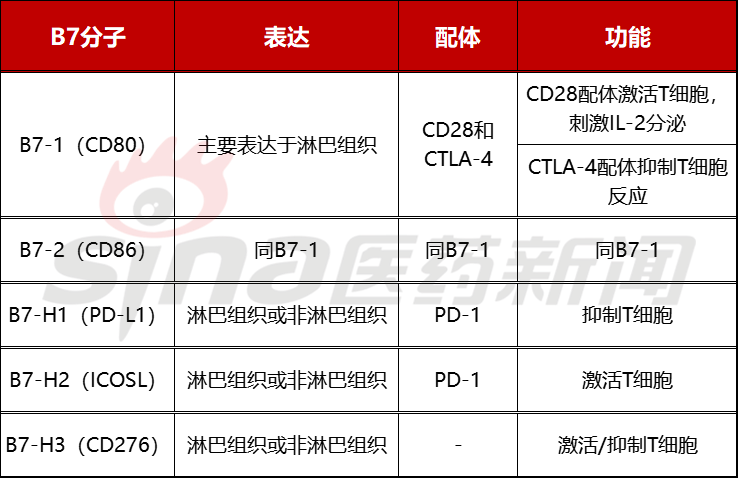
B7-H3又名CD276,是B7重要的家庭免疫检查点分子。B7-H3主要表现在纤维细胞、内皮细胞、成骨细胞等非免疫细胞表面,以及激活细胞APC、NK研究表明,B7-H3表达在黑色素瘤、白血病、乳腺癌、前列腺癌等肿瘤表面,与肿瘤的生长、转移、复发和预后不良密切相关。B7-H3在小鼠模型中,髓样细胞受体家族中表达的触发受体尚未被发现。TLT-2被认为是小鼠B7-H3潜在受体。
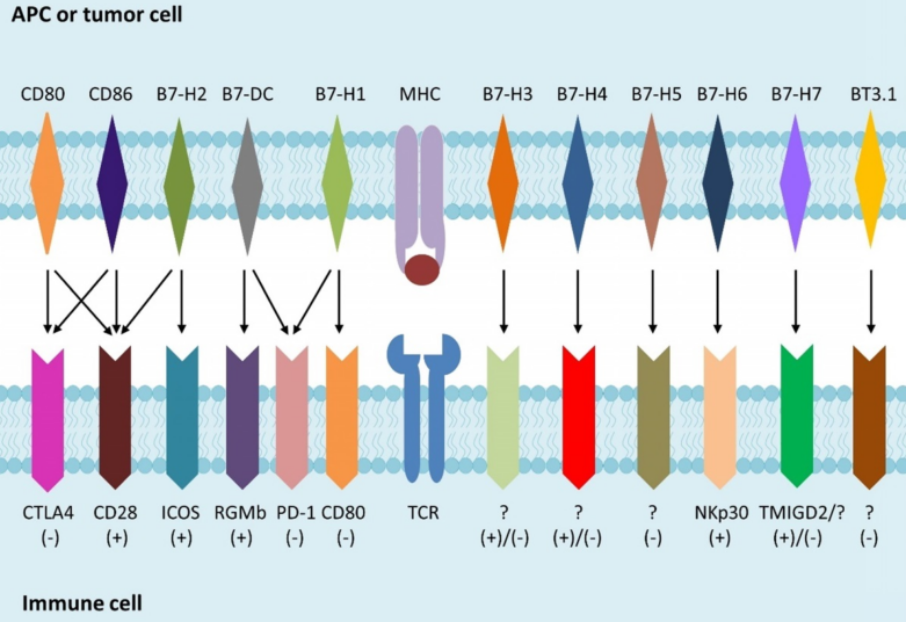
图:B7家族示意图
目前,B7-H3确切机制仍不清楚,但被认为是参与共刺激和共抑制的途径。一方面,早期研究认为,早期研究认为,早期研究认为,共刺激和共抑制的途径。B7-H3共同刺激受体,促进CD4 和CD8 T细胞增殖刺激干扰素γ(IFN-γ)另一方面,近年来越来越多的研究表明,B7-H3为了共同抑制受体,通过抑制受体,T细胞的抑制作用,在肿瘤免疫逃逸中发挥作用。目前,针对目前,针对目前,对于肿瘤免疫逃逸。B7-H3靶点药物开发主要是靶点药物开发B7-H3抑制剂,通过对B7-H3实现抗肿瘤作用的特异性阻断。

图:B7-H3介导的信号通路
数据来源:《Int J Biol Sci》
02
靶向B7-H3药物正在研究现状
尽管B7-H3分子机制尚不清楚,但作为一种潜在的免疫检查点,肿瘤免疫治疗的前景备受关注。目前,针对目前的目标,针对目前的肿瘤免疫治疗。B7-H3靶点的开发涉及单抗、双抗、ADC、CAR-T等药物。
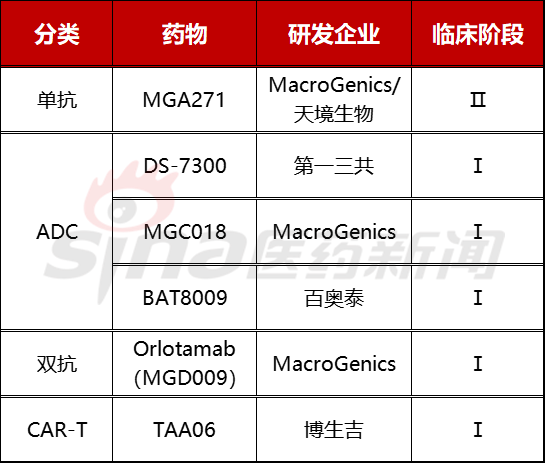
(1)单抗
MGA271(enoblituzumab)是MacroGenics公司开发的人源化公司B7-H3单抗,目前正处于临床实践中Ⅱ期。MGA271基于MacroGenics的Fc优化平台研发,优化抗原结合片段B7-H3高亲和力,通过ADCC发挥抗肿瘤作用。Fc增强和激活优化技术CD16A FcγR亲和力降低和抑制性FcγR CD32B亲和力,强化诸如ADCC等效应功能。
在一项Ⅰ期研究(NCT01391143)中,enoblituzumab耐受剂量高达15mg/kg,确认安全性好,未导致药物相关不良反应停止研究(TRAE)。
enoblituzumab与PD-1抑制剂联合使用前景良好。2018年 SITC上,MacroGenics公布了Enoblituzumab联合帕博利珠单抗的临床数据。Ⅰ/Ⅱ临床试验表明(NCT02475213),与单独使用抗PD-1与阻断方法相比,enoblituzumab与帕博利珠单抗联用组的总缓解率几乎翻了一番。头颈鳞状癌。(SCCHN),联用组实现33.3客观缓解率为%,对于非小细胞肺癌,联用组实现35.7客观缓解率为%。安全方面,27.1%的患者(N = 133)经历了3级以上的经历AE,6.8%的患者因AE退出后,一名患者死于肺炎不良事件。一般来说,联合治疗和联合治疗。PD-1抑制剂单药疗法TRAE相当。

图:enoblituzumab与PD-1抑制剂总缓解率翻倍
数据来源:MacroGenics
除了与PD-1除单抗联用外,MGA271与伊匹木单抗(CTLA-4)、以及PD-1和LAG-3双特异性抗体(tebotelimab)联合疗法(NCT04634825)临床试验正在进行中。
2019七月,天境生物与MacroGenics签署协议,共同开发和商业化enoblituzumab,天境生物将主导大中华区enoblituzumab参与临床开发和销售,参与临床开发和销售,参与MacroGenics主导的全球临床研发。MacroGenics将获得1500万美元的首付款,同时可能获得不高于1500万美元的首付款1.35潜在开发和注册里程碑支付1亿美元。

图:Enoblituzumab示意图
数据来源:MacroGenics
(2)ADC药物
DS-7300是第一三共研发的靶向B7-H3的ADC药物,目前正处于临床实践中Ⅰ期。DS-7300也是基于第一三共专利的ADC平台——DXd-ADC研发。DS-7300包括三个部分,一个是靶向B7-H3的IgG1单抗,二是四肽可裂解Linker,三是DNA拓扑异构酶抑制剂DXd,DAR=4。
在2021 ESMO上面,第三共公布了DS-7300的Ⅰ早期数据,在70例晚期肿瘤患者中,客观缓解率达到21.42%,包括10例部分缓解患者和5例待确认部分缓解患者,另外32例报告了疾病稳定性(SD=45.71%)。安全方面,未观察到剂量限制性毒性,31.4%%3级及以上患者出现3级及以上患者出现3级及以上患者出现3级及以上患者出现TRAE,最常见的是贫血和淋巴细胞计数下降。
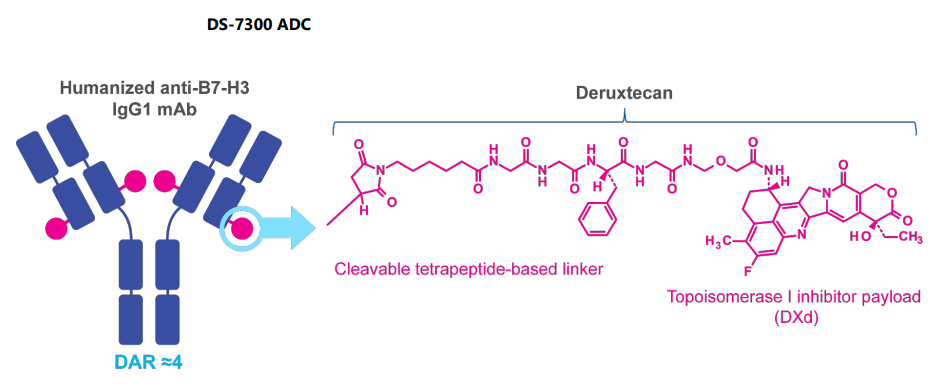
图:DS-7300示意图
数据来源:第一三共
MGC018是MacroGenics研究的目标B7-H3 ADC药物,由抗B7-H3人源化IgG1单抗经可裂解Linker偶联Duocarmycin(DUBA)形成,平均DAR为2.7。DUBA是一种DNA烷化剂,靶向DNA小沟,可引起DNA双链断裂。
在2021 ESMO上,MacroGenics公布了MGC018治疗晚期实体瘤Ⅰ期临床试验(cohort expansion,NCT03729596),该测试包括86名患者,包括40名前列腺癌、21名非小细胞肺癌、16名三阴乳腺癌和9名黑色素瘤患者。共有37名患者退出了测试,包括25名疾病进展(PD),6名患者因AE退出,一人因医生意见退出,一人因死亡退出。安全方面,43名患者出现3级及以上。TRAE(50%),常见严重TRAE包括中性粒细胞减少(22.1%)和血小板减少(7%)。疗效方面,在32名可评估患者中,客观缓解率为25%(8/32),均为部分缓解,包括4名前列腺癌患者和4名非小细胞肺癌患者。总的来说,MGC018治疗前列腺癌和非小细胞肺癌前景良好,但安全性值得进一步探索,目前,MacroGenics正在进一步优化MGC018初始剂量。
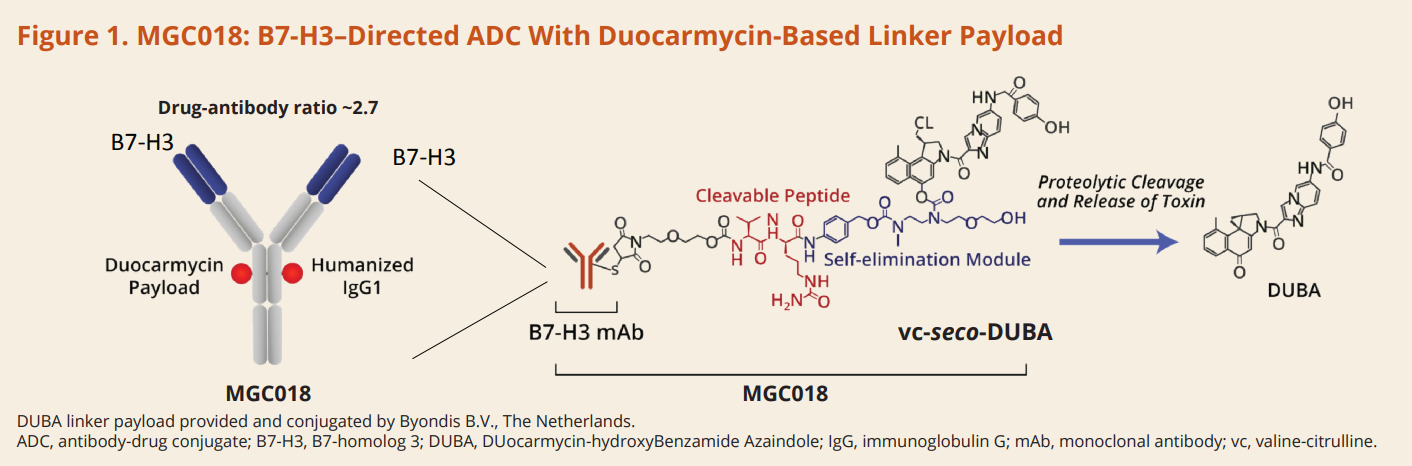
图:MGC017示意图
数据来源:MacroGenics
聚焦国内,百奥泰BAT8009是一款B7-H3 ADC该药物于2020年4月15日获批临床实践,该药物是由重组人源化抗抗重组而成的B7-H3抗体与DNA拓扑异构酶抑制剂由可裂解连接子偶联而成,具有旁观者效应。
(3)双抗药物
Orlotamab(MGD009)是由MacroGenics研发人源化、双特异性DART分子,可同时识别CD3和B7-H3,通过T杀死细胞的重定位B7-H3肿瘤细胞的表达。DART技术为MacroGenics公司的专利技术是一种由两个多肽链组合而成的异源二聚体抗体。首先使用Linker抗体可变区分别为抗体可变区VL、VH与另一个抗体可变区相同VL、VH形成序列连接scFv,之后共表达了两个scFv片段,使用抗体VH和VL结构域链相互作用形成双特异片段。与结构域链相互作用。BiTE平台相比,DART该平台具有更好的结构和生物学特性,包括更好的稳定性和生物学特性T更好地重定向恶性细胞的细胞毒性作用。
2018年,Orlotamab因肝脏不良事件FDA部分暂停(Partial clinical hold),随后于2019年1月宣布暂停移除。近年来,公司未披露。Orlotamab值得一提的是,公司研发管道中没有临床进展Orlotamab可能与肝毒性不良事件有关。
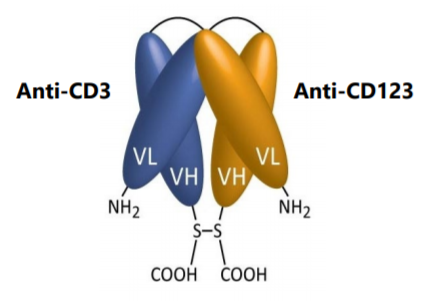
图:DART双抗分子示意图
数据来源:MacroGenics
(4)CAR-T细胞疗法
TAA06注射液是博生吉医药科技有限公司研发的靶向注射液B7-H3 CAR-T细胞疗法。2022年3月21日,博生吉医药科技有限公司宣布,TAA06注射液获FDA授予的孤儿药物资格用于治疗神经母细胞瘤。此外,斯坦福大学和哈佛大学的科学家在小鼠模型中进行了小鼠模型B7-H3 CAR-T观察到细胞的治疗B7-H3 CAR-T它能明显抑制小鼠肿瘤的生长,延长小鼠的生存期。
03
小结
尽管B7-H3分子机制尚不清楚,但作为一种潜在的免疫检查点,肿瘤免疫治疗的前景备受关注。MacroGenics公司深耕于B7-H3靶点,研究药物涉及单抗、双抗和ADC,由于肝毒性问题,双抗产品在临床试验中受到影响FDA暂停,目前在公司研发管道中很难找到痕迹。单抗产品。enoblituzumab与PD-1抑制剂联合使用前景良好,头颈鳞癌和非小细胞肺癌客观缓解率翻倍。世界各地的抑制剂联合使用前景良好。ADC第一、三共领军企业也非常青睐这一目标,DS-7300沿用了Trop2 ADC产品DS-1062设计。聚焦国内、天生生物License in enoblituzumab;百奥泰再战B7-H3 ADC;博生吉靶向B7-H3的CAR-T细胞疗法获FDA孤儿药资格认定。一般来说,B7-H3目标整体呈现百花齐放的局面,谁将脱颖而出,让我们拭目以待。
