阿斯利康AZD批准8205临床试验申请
发布时间: 2022-06-15 13:44:02
6月14日,CDE阿斯利康官网显示AZD治疗晚期或转移性实体恶性肿瘤的8205临床试验申请获得批准。HS-20089后,国内第二批临床批准B7-H4抗体偶联药物(ADC)。
细胞表面糖蛋白B7-H4.肿瘤免疫治疗的潜在目标是在一系列实体瘤中表达,如乳腺癌、卵巢癌、子宫内膜癌和胆管癌。
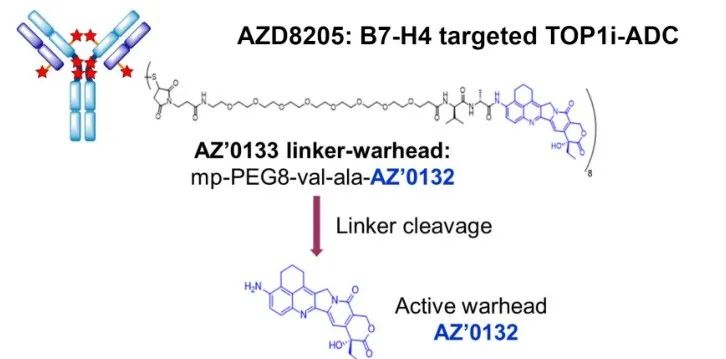
AZD8205是一款B7-H4靶向ADC,新型拓扑异构酶1抑制剂(TOP1i)—linker—靶向B7-H4的抗体组成。它的作用机制是TOP1i弹头递送至B7-H导致4阳性细胞DNA受伤和细胞死亡。
根据阿斯利康2022AACR会议摘要披露,在一个项目中有26个案例TNBC PDX3.肿瘤模型研究.5 mg/kg AZD8205单静脉注射单次静脉注射(IV)给药的总缓解率为69%(肿瘤比基线消退)≥其中完全缓解率为36%(9/26)。进一步的分析表明,B7-H4表达上升及DNA损伤修复 (DDR)在缺陷模型中观察到更强的抗肿瘤活性。
阿斯利康目前正在研究中ADC多达12种产品,涉及目标,包括HER2、TROP2、CD25、PCMA等。
原名:阿斯利康B7-H4 ADC在国内获批临床

